
Wetenschap
Vorming van ammoniumchloride:inzicht in de reactielocatie
1. Verspreidingssnelheden:
* Ammoniak (NH₃) is lichter dan HCl: Ammoniakgas heeft een lager molecuulgewicht dan waterstofchloride. Dit betekent dat ammoniakmoleculen sneller bewegen en sneller door de lucht diffunderen.
* HCl diffundeert langzamer: HCl is zwaarder en diffundeert langzamer.
2. De reactie:
* Ammoniak en HCl reageren in de lucht: Wanneer ammoniak- en HCl-gasmoleculen botsen, reageren ze onder vorming van ammoniumchloride (NH₄Cl). Deze reactie is exotherm (er komt warmte vrij).
3. Het resultaat:
* Meer botsingen nabij het HCl-einde: Omdat HCl langzamer diffundeert, duurt het langer om zich te verspreiden. Dit betekent dat er een hogere concentratie HCl-moleculen is nabij het HCl-uiteinde van de buis.
* Meer botsingen betekenen meer ammoniumchloride: Omdat er meer HCl dichter bij het HCl-uiteinde zit, vinden er meer botsingen plaats, wat resulteert in meer ammoniumchloridevorming nabij die locatie.
In wezen vormt het ammoniumchloride zich dichter bij het HCl-uiteinde omdat het HCl-gas langzamer diffundeert en daardoor een dichtere wolk van HCl-moleculen creëert waarmee de ammoniak kan reageren.
 Worden christenen ‘groener’?
Worden christenen ‘groener’?  Wat is de betekenis van licht?
Wat is de betekenis van licht?  'Alsof je leven op Mars vindt':waarom de ondergrondse orchidee de vreemdste, meest mysterieuze bloem van Australië is
'Alsof je leven op Mars vindt':waarom de ondergrondse orchidee de vreemdste, meest mysterieuze bloem van Australië is  Tropische cycloon Debbie heeft een gat geslagen in de Australische aanvoer van wintergroenten
Tropische cycloon Debbie heeft een gat geslagen in de Australische aanvoer van wintergroenten Dinosaurussen leefden in een kasklimaat met hete zomers
Dinosaurussen leefden in een kasklimaat met hete zomers
Hoofdlijnen
- Reproductie in bryophyllum vindt plaats in?
- Wanneer zijn dinosaurussen uitgestorven? De theorieën over hoe het gebeurde en wat het overleefde
- Wat zijn de drie basistypen van wetenschappelijke observatie?
- Colombia wordt de eerste case study over hoe biodiversiteitsdoelstellingen in evenwicht kunnen worden gebracht met beperkte economische middelen
- Wat is de naam van het stadium A -cel totdat net voorafgaand aan mitose?
- Welke opslaginformatie maakt eiwit en reguleert de reproductie van celgroei?
- Wat is Phlostigen?
- Wat zijn de belangrijkste feiten over oogenese?
- Maakt Ancestry deel uit van een omgeving?
- Hoe hitte en zonlicht het chloorniveau in het zwembad beïnvloeden

- Adsorberend materiaal ontwikkeld uit PET-flessen voor het verwijderen van antibiotica uit water
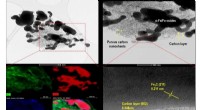
- Onderzoekers kunnen nu snel nauwkeurig scannen op nutriëntengehalte in het gangpad met producten

- Een nieuwe methode voor ononderbroken monitoring van freesreacties in vaste toestand

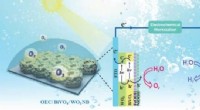
- Verbetering van de prestaties voor efficiënte foto-elektrochemische watersplitsing
 Hoe worden krachten in een vloeistof overgedragen?
Hoe worden krachten in een vloeistof overgedragen?  Wat zijn twee voorbeelden van externe factoren die de celcyclus beïnvloeden?
Wat zijn twee voorbeelden van externe factoren die de celcyclus beïnvloeden?  Weet je het niet zeker? Maak je geen zorgen:omarm onzekerheid
Weet je het niet zeker? Maak je geen zorgen:omarm onzekerheid  Hoe de periode van de pendel te berekenen
Hoe de periode van de pendel te berekenen Hoe zijn peptiden en eiwitten vergelijkbaar?
Hoe zijn peptiden en eiwitten vergelijkbaar?  Wat zijn de homofoons voor een elektrische flits van wolken en lichter worden?
Wat zijn de homofoons voor een elektrische flits van wolken en lichter worden?  Wat denken werkgevers in Londen werkelijk over hybride werken?
Wat denken werkgevers in Londen werkelijk over hybride werken?  Alternatieve oplosmiddelen voor benzeen
Alternatieve oplosmiddelen voor benzeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

