
Wetenschap
Empirische en moleculaire formules begrijpen:een eenvoudige gids
Zo kun je het begrijpen:
* Empirische formule: Vertegenwoordigt de eenvoudigste gehele getalsverhouding van atomen in een verbinding. Het vertelt je niet noodzakelijkerwijs het exacte aantal atomen in een molecuul, maar het geeft de relatieve verhoudingen weer.
* Moleculaire formule: Vertegenwoordigt het werkelijke aantal atomen van elk element in een molecuul.
Voorbeeld:
* Glucose: De molecuulformule is C₆H₁₂O₆, wat betekent dat het 6 koolstof-, 12 waterstof- en 6 zuurstofatomen heeft.
* Empirische formule van glucose: CH₂O (eenvoudigste gehele getalverhouding van 1:2:1).
Empirische formule bepalen:
1. Vind de massa van elk element in de verbinding. Dit kan experimenteel worden gedaan of in het probleem worden vermeld.
2. Convert de massa's om naar mol met behulp van de molaire massa van elk element.
3. Deel het aantal mol van elk element door het kleinste aantal mol. Dit geeft je de eenvoudigste gehele getalsverhouding van atomen.
4. Als de resulterende getallen geen gehele getallen zijn, vermenigvuldig ze dan met het kleinste gehele getal waardoor ze allemaal geheel zijn.
Belangrijkste punt: De empirische formule is essentieel voor het begrijpen van de samenstelling van een verbinding. Het helpt onbekende verbindingen te identificeren en hun eigenschappen te voorspellen.
 Hoe de K-waarde op een titratiegrafiek te berekenen
Hoe de K-waarde op een titratiegrafiek te berekenen  Nieuwe verbindingen met gesynthetiseerde anticarcinogene verbindingen
Nieuwe verbindingen met gesynthetiseerde anticarcinogene verbindingen Leg uit door kinetische moleculaire theorie waarom ijs dichter is dan waterdampen?
Leg uit door kinetische moleculaire theorie waarom ijs dichter is dan waterdampen?  Welk bewijs is er dat kaliumferrocyanide en ijzerchloride diffunderen met dezelfde snelheid?
Welk bewijs is er dat kaliumferrocyanide en ijzerchloride diffunderen met dezelfde snelheid?  Wordt een term gebruikt om een elektrisch neutraal molecuul gevormd te worden gevormd door covalente bindingen tussen atomen die dezelfde elektronegativiteit hebben?
Wordt een term gebruikt om een elektrisch neutraal molecuul gevormd te worden gevormd door covalente bindingen tussen atomen die dezelfde elektronegativiteit hebben?
 Welke 14 bomen hebben het hele jaar door blad?
Welke 14 bomen hebben het hele jaar door blad?  Ecologisch belang van algae
Ecologisch belang van algae De verschillen tussen een poema, een poema en een bergleeuw
De verschillen tussen een poema, een poema en een bergleeuw Een aardbeving met een kracht van 7,1 op de schaal van Richter treft de kust van Indonesië
Een aardbeving met een kracht van 7,1 op de schaal van Richter treft de kust van Indonesië Klimaatverandering zal de komende decennia miljoenen verdringen - landen moeten zich nu voorbereiden om hen te helpen
Klimaatverandering zal de komende decennia miljoenen verdringen - landen moeten zich nu voorbereiden om hen te helpen
Hoofdlijnen
- Welke zuren zijn te vinden in het menselijk lichaam?
- Hoe een organisme problemen met osmose overwint?
- Wetenschappers ontdekken hoe het klokgen groene algen wakker maakt
- Wat is de klasse van clubschimmels?
- Wat is biochemische vergelijking?
- Zijn sekscellen van een mannelijk en vrouwelijk bekend als gameten?
- Wat zijn de voordelen van het gebruik van micro -organismen boven dieren en planten?
- Wat doet de verkeerde pH om een enzym vorm te geven?
- Onderzoek naar de genetica van kleurenblindheid:een stapsgewijs wetenschapsbeursproject
- Een betere bouwsteen voor het maken van nieuwe materialen
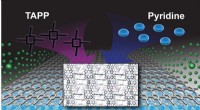
- Onderzoek kan ertoe bijdragen dat flexibele technologie langer meegaat, vermijd kritieke storingen

- 4D-weefsels cultiveren - het zelfgebogen hoornvlies
- AlScN – alternatief materiaal voor efficiëntere smartphonehardware

- Nieuw, vereenvoudigde techniek maakt licht metalen nanofoam

 Heeft Archaea een celmembraan?
Heeft Archaea een celmembraan?  Op welke eigenschappen zijn stralende energie vergelijkbaar?
Op welke eigenschappen zijn stralende energie vergelijkbaar?  Leg uit waarom de elektrische lading op een atoom nul of neutraal is?
Leg uit waarom de elektrische lading op een atoom nul of neutraal is?  Voorspellend vermogen:een robot die jouw intentie leest? (met video)
Voorspellend vermogen:een robot die jouw intentie leest? (met video)  Waarom gaat de batterij van mijn telefoon zo snel leeg?
Waarom gaat de batterij van mijn telefoon zo snel leeg? Hoe snel reist licht door waterstof?
Hoe snel reist licht door waterstof?  Hoe verklaart de principe Bunsen Burner?
Hoe verklaart de principe Bunsen Burner?  Welk macro -molecuul bevat enzymen?
Welk macro -molecuul bevat enzymen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

