
Wetenschap
Chemische structuren tekenen:een uitgebreide gids
1. Begrijp de basisprincipes
* Atomen: De fundamentele bouwstenen van alle materie. Ze bestaan uit een kern (die protonen en neutronen bevat) en elektronen die om de kern draaien.
* Elementen: Zuivere stoffen die uit slechts één type atoom bestaan (bijvoorbeeld waterstof, koolstof, zuurstof).
* Verbindingen: Stoffen die worden gevormd wanneer twee of meer verschillende elementen chemisch worden gecombineerd (bijvoorbeeld water, koolstofdioxide).
* Chemische formules: Geef de soorten en aantallen atomen in een verbinding weer (bijvoorbeeld H₂O voor water, CO₂ voor koolstofdioxide).
2. Bepaal de elementen en hun aantal
* Chemische formule: Begin met de chemische formule van de verbinding. Dit vertelt u welke soorten elementen aanwezig zijn en hun hoeveelheden.
* Voorbeeld: Water (H₂O) heeft twee waterstofatomen (H) en één zuurstofatoom (O).
3. Begrijp binding
* Covalente binding: Atomen delen elektronen om een stabiele elektronenconfiguratie te bereiken. Dit is het meest voorkomende type binding in organische verbindingen.
* Ionische binding: Het ene atoom draagt elektronen over aan het andere, waardoor ionen ontstaan met tegengestelde ladingen die elkaar aantrekken. Dit komt vaak voor bij anorganische verbindingen.
4. Teken de skeletstructuur
* Centraal Atoom: Vaak zal het minst elektronegatieve atoom (het atoom met de lagere neiging om elektronen aan te trekken) het centrale atoom zijn.
* Connectiviteit: Verbind de atomen in de verbinding op basis van de chemische formule en bindingsregels.
* Voorbeeld: In methaan (CH₄) is koolstof (C) het centrale atoom, dat gebonden is aan vier waterstofatomen (H).
5. Voeg elektronen en alleenstaande paren toe
* Valentie-elektronen: Het aantal elektronen in de buitenste schil van een atoom.
* Octetregel: De meeste atomen streven ernaar om acht elektronen in hun buitenste schil te hebben (uitzonderingen:waterstof en helium).
* Eenzame paren: Paren elektronen die niet betrokken zijn bij binding. Deze worden vaak getekend als stippen rond een atoom.
6. Overweeg moleculaire geometrie
* Vorm: De rangschikking van atomen in de driedimensionale ruimte. Moleculaire geometrie beïnvloedt de eigenschappen van de verbinding.
* VSEPR-theorie: Deze theorie helpt moleculaire vormen te voorspellen op basis van de afstoting van elektronenparen.
Voorbeeld:de atomaire structuur van water tekenen (H₂O)
1. Chemische formule: H₂O
2. Elementen: Waterstof (H) en zuurstof (O)
3. Verbinding: Covalente binding (delen van elektronen)
4. Skelet: O in het midden, verbonden met twee H-atomen.
5. Elektronen: Zuurstof heeft 6 valentie-elektronen, waterstof heeft er 1. Zuurstof vormt twee covalente bindingen met waterstof, waardoor er 2 vrije elektronenparen op het zuurstofatoom achterblijven.
6. Moleculaire geometrie: Water heeft een gebogen vorm vanwege de afstoting tussen de alleenstaande elektronenparen en de bindende elektronenparen.
Tips voor het tekenen van atomaire structuren:
* Gebruik een potlood: Dit maakt eenvoudig wissen en corrigeren mogelijk.
* Gebruik een richtliniaal: Voor precieze lijnen.
* Label atomen en bindingen: Zo houd je de structuur in de gaten.
* Oefenen: Het tekenen van atomaire structuren vergt oefening. Begin met eenvoudige verbindingen en werk geleidelijk toe naar complexere verbindingen.
* Bronnen: Gebruik leerboeken, online tutorials en andere bronnen om meer te leren over atomaire structuren en bindingen.
Softwaretools
* ChemDraw: Krachtige software voor het tekenen van chemische structuren.
* MarvinSketch: Gratis online tekentool.
Bedenk dat het tekenen van de atomaire structuur van een verbinding een essentiële vaardigheid in de scheikunde is. Door de basisbeginselen te begrijpen en te oefenen, kunt u met vertrouwen de structuur van verschillende moleculen weergeven.
 PH niveaus van fruit
PH niveaus van fruit  Hoe kernbommen werken
Hoe kernbommen werken  Van welk nut is natriumchloraat?
Van welk nut is natriumchloraat?  Hoeveel zuurstofatomen zitten er in deze formule Al2SO43?
Hoeveel zuurstofatomen zitten er in deze formule Al2SO43?  Het proces van het splitsen van water om hydrogenen en elektronen af te geven, treedt op tijdens de A -lichtafhankelijke B onafhankelijke C koolstoffixatie D fotofosforylering E glyc?
Het proces van het splitsen van water om hydrogenen en elektronen af te geven, treedt op tijdens de A -lichtafhankelijke B onafhankelijke C koolstoffixatie D fotofosforylering E glyc?
 Eenvoudige zelfgemaakte weerinstrumenten voor kinderen
Eenvoudige zelfgemaakte weerinstrumenten voor kinderen Wat betekent wetenschappelijke integriteit?
Wat betekent wetenschappelijke integriteit?  Hoe beïnvloedt ontbossing de lucht?
Hoe beïnvloedt ontbossing de lucht?  Vier harde acties die zouden helpen de wereldwijde plasticcrisis te bestrijden
Vier harde acties die zouden helpen de wereldwijde plasticcrisis te bestrijden Nieuw onderzoek suggereert dat het klimaatdoel van 1,5C onbereikbaar zal zijn zonder groenere herstelplannen voor COVID-19
Nieuw onderzoek suggereert dat het klimaatdoel van 1,5C onbereikbaar zal zijn zonder groenere herstelplannen voor COVID-19
Hoofdlijnen
- Welke moleculen bepalen de weefselspecificiteit van hormonen?
- Is dit een organel die eiwitten voor de cel samenstelt?
- Waarom mensen schreeuwen,
- Waarom oudere vaders meer genetische mutaties doorgeven aan hun nakomelingen
- Nieuwe biobronnen voor plantaardige peptidehormonen met behulp van technologie voor het bewerken van genen
- Wat is het deel van het enzym in welke stof past?
- Amazoneboeren ontdekten het geheim van het domesticeren van wilde rijst 4, 000 jaar geleden
- Waar bevindt de functionele eenheid van het oor zich?
- Wat is condrogenese?
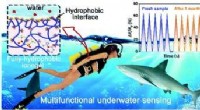
- Volledig hydrofobe ionogel ontwikkeld voor draagbare onderwatersensor en communicator
- Zijn groene huishoudelijke consumentenproducten minder giftig dan traditionele producten?

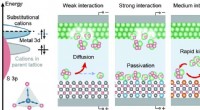
- Vulkaanvormige trend maakt rationeel ontwerp van polysulfidekatalysatoren in lithium-zwavelbatterijen mogelijk
- Eck Industries licentieert exclusief cerium-aluminiumlegering mede ontwikkeld door ORNL

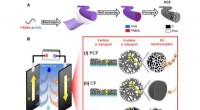
- Poreuze koolstofnanovezels vertonen uitzonderlijke capacitieve deïonisatie
 Fakkels in beweging:testkit voor nanodeeltjes laat zien hoe nanodeeltjes van verschillende grootte zich verspreiden in tumorweefsel
Fakkels in beweging:testkit voor nanodeeltjes laat zien hoe nanodeeltjes van verschillende grootte zich verspreiden in tumorweefsel Wat zijn de voordelen en desvantadges van het zingen van een thermorcouple in plaats daarvan reguliere laboratoriumthermometer?
Wat zijn de voordelen en desvantadges van het zingen van een thermorcouple in plaats daarvan reguliere laboratoriumthermometer?  Facebook schort 200 apps op wegens datamisbruik (update)
Facebook schort 200 apps op wegens datamisbruik (update) Wat is een substantie die kneedbaar en solide bij kamertemperatuur kneed?
Wat is een substantie die kneedbaar en solide bij kamertemperatuur kneed?  Hoe Indiase vrouwen in Australië familiaal geweld ervaren en hoe het te bestrijden
Hoe Indiase vrouwen in Australië familiaal geweld ervaren en hoe het te bestrijden Fiat Chrysler-manager aangeklaagd in Amerikaanse dieselemissiezaak
Fiat Chrysler-manager aangeklaagd in Amerikaanse dieselemissiezaak Wat is de relatie tussen diameter van planeten en hun posities van de zon?
Wat is de relatie tussen diameter van planeten en hun posities van de zon?  Sleutelinstrument op NASA's InSight-lander zit vast. Een Martiaanse rots kan de schuld zijn
Sleutelinstrument op NASA's InSight-lander zit vast. Een Martiaanse rots kan de schuld zijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

