
Wetenschap
Chemische bindingen begrijpen:hoe elektronegativiteit een rol speelt
Elektronegativiteit:
* Definitie: Elektronegativiteit is de maatstaf voor het vermogen van een atoom om elektronen naar zichzelf toe te trekken wanneer het zich in een chemische binding bevindt.
* Trends: Elektronegativiteit neemt over het algemeen toe over een bepaalde periode (van links naar rechts) en neemt af in een groep (van boven naar beneden) in het periodiek systeem.
Bondtypes en verschillen in elektronegativiteit:
* Niet-polaire covalente obligaties: Wanneer het elektronegativiteitsverschil tussen twee atomen erg klein is (meestal minder dan 0,5), worden de elektronen gelijkelijk verdeeld. Hierdoor ontstaat een niet-polaire covalente binding. Voorbeeld:Cl-Cl in chloorgas (Cl₂).
* Polaire covalente obligaties: Wanneer het elektronegativiteitsverschil tussen twee atomen gematigd is (tussen 0,5 en 1,7), worden de elektronen ongelijk verdeeld. Hierdoor ontstaat een polaire covalente binding, waarbij het ene atoom een licht negatieve lading heeft (δ-) en het andere een licht positieve lading heeft (δ+). Voorbeeld:H-Cl in waterstofchloride (HCl).
* Ionische bindingen: Wanneer het elektronegativiteitsverschil tussen twee atomen groot is (groter dan 1,7), worden de elektronen in wezen overgedragen van het ene atoom naar het andere. Hierdoor ontstaat een ionische binding, wat resulteert in een positief geladen kation en een negatief geladen anion. Voorbeeld:Na-Cl in natriumchloride (NaCl).
Elektronegativiteit gebruiken om bindingstypen te bepalen:
1. Zoek de elektronegativiteitswaarden: Zoek de elektronegativiteitswaarden op van de twee atomen in kwestie. Je kunt deze waarden vinden in een leerboek, online of op het periodiek systeem.
2. Bereken het verschil: Trek de kleinere elektronegativiteitswaarde af van de grotere.
3. Interpreteer het verschil:
* Verschil <0,5:niet-polaire covalente binding
* 0,5
Belangrijke overwegingen:
* Bondpolariteit: Hoe groter het elektronegativiteitsverschil, hoe polairder de binding. Dit betekent dat er een grotere scheiding van lading tussen de atomen is.
* Verbindingssterkte: Ionische bindingen zijn doorgaans sterker dan covalente bindingen vanwege de volledige overdracht van elektronen.
* Uitzonderingen: Er zijn enkele uitzonderingen op deze regels, vooral voor elementen in het midden van het periodiek systeem.
Voorbeeld:
Laten we eens kijken naar de binding in koolstofdioxide (CO₂).
* Elektronegativiteit van koolstof (C):2,55
* Elektronegativiteit van zuurstof (O):3,44
Verschil =3,44 - 2,55 =0,89
Het elektronegativiteitsverschil ligt tussen 0,5 en 1,7, dus de bindingen in CO₂ zijn polair covalent .
 De knoestige kwestie van het aroma van zachte krakeling oplossen
De knoestige kwestie van het aroma van zachte krakeling oplossen Wat is de naam van covalente verbinding P2O5?
Wat is de naam van covalente verbinding P2O5?  Kaliumoxide- en waterreactie:chemische vergelijking en uitleg
Kaliumoxide- en waterreactie:chemische vergelijking en uitleg  Wat is de hoeveelheid opgeloste stof die in 100 g oplosmiddel kan oplossen?
Wat is de hoeveelheid opgeloste stof die in 100 g oplosmiddel kan oplossen?  Azoxymethaan (AZOXYMETHaan) Lewis-structuur:een stapsgewijze handleiding
Azoxymethaan (AZOXYMETHaan) Lewis-structuur:een stapsgewijze handleiding
 In de wind waaien - het plasticprobleem uit elkaar halen
In de wind waaien - het plasticprobleem uit elkaar halen Waarom worden de archeebacteriën en eubacteriën gevonden aan de onderkant van de fylogenie -boom?
Waarom worden de archeebacteriën en eubacteriën gevonden aan de onderkant van de fylogenie -boom?  Loofbomen:kenmerken en waarom ze hun bladeren verliezen
Loofbomen:kenmerken en waarom ze hun bladeren verliezen  Verblind door het licht:klimaatverandering, de zon, en Lake Superior
Verblind door het licht:klimaatverandering, de zon, en Lake Superior Vertragen:Nederlanders verlagen maximumsnelheid om vervuiling in te dammen
Vertragen:Nederlanders verlagen maximumsnelheid om vervuiling in te dammen
Hoofdlijnen
- Wat is het doel van lysosomen?
- Hebben alle cellen dezelfde samenstelling?
- De tak van de biologie die zowel het diversiteits- als de eenheidsleven verklaart?
- Waar is glucoseproducten voor?
- Waarom treedt cellysis voor voor dieren, geen plantencel?
- Interfase, metafase en anafase begrijpen:sleutelfasen van de celcyclus
- De biologische verklaring voor hoe geheugen werkt wordt genoemd?
- De mannelijke reproductieve structuur van niet -vasculaire planten wordt genoemd?
- Groeien en delen alle cellen tegelijkertijd?
- Onderzoekers synthetiseren hernieuwbare oliën voor gebruik in smeermiddelen

- Nieuwe technologie kan helpen water af te stoten, levens redden door verbeterde medische hulpmiddelen

- Onderzoekers identificeren een metaal dat bestand is tegen ultrahoge temperatuur en druk

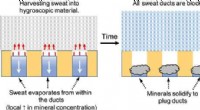
- Het zweet tegen zichzelf keren met een metaalvrije anti-transpirant
- Gerecycled katoen wordt nieuwe stof

 Wanneer fossiele brandstoffen worden verbrand, wat is bedekt met kinetische energie?
Wanneer fossiele brandstoffen worden verbrand, wat is bedekt met kinetische energie?  Wat zijn de verschillende wetenschappelijke methoden en verklaren?
Wat zijn de verschillende wetenschappelijke methoden en verklaren?  Synthese van een in water oplosbaar kromgetrokken nanograafeen en de toepassing ervan voor foto-geïnduceerde celdood
Synthese van een in water oplosbaar kromgetrokken nanograafeen en de toepassing ervan voor foto-geïnduceerde celdood Beheers de vergelijking om kwantumtechnologieën te stimuleren
Beheers de vergelijking om kwantumtechnologieën te stimuleren Wat is het verband tussen analytische lijnen en statische compositie?
Wat is het verband tussen analytische lijnen en statische compositie?  Mede-oprichter van Apple zegt dat Goldmans Apple Card-algo discrimineert
Mede-oprichter van Apple zegt dat Goldmans Apple Card-algo discrimineert Vrijstaande anode voor gebruik bij het helpen van microbiële brandstofcellen om afval om te zetten in elektriciteit
Vrijstaande anode voor gebruik bij het helpen van microbiële brandstofcellen om afval om te zetten in elektriciteit Betelgeuze blijft zich mysterieus gedragen. Dit is wat er zou gebeuren als het zou ontploffen
Betelgeuze blijft zich mysterieus gedragen. Dit is wat er zou gebeuren als het zou ontploffen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

