
Wetenschap
Ionische verbindingen:kristalstructuur, smeltpunten en elektrische geleidbaarheid
* Ordentelijke kristalvormen: Ionische verbindingen vormen kristalroosters, die zeer geordende en zich herhalende driedimensionale structuren zijn. Daarom vertonen ze vaak goed gedefinieerde, geometrische vormen.
* Hoge smeltpunten: Ionische verbindingen hebben sterke elektrostatische aantrekkingen tussen hun tegengesteld geladen ionen. Het overwinnen van deze attracties vergt veel energie, wat leidt tot hoge smeltpunten.
* Elektrische geleidbaarheid bij oplossing in water: Wanneer ionische verbindingen in water oplossen, kunnen hun ionen vrij bewegen. Hierdoor kan de oplossing elektriciteit geleiden.
Samengevat: Ja, ordelijke kristalvormen, hoge smeltpunten en elektrische geleidbaarheid bij oplossing in water zijn allemaal eigenschappen die kenmerkend zijn voor ionische verbindingen.
Belangrijkste afhaalpunten: Deze eigenschappen zijn het resultaat van de sterke elektrostatische krachten die de ionen in de vaste toestand bij elkaar houden en hun vermogen om te dissociëren en vrij in oplossing te bewegen.
 Welke term beschrijft het beste het aantal individuen van een bepaalde soort per oppervlakte-eenheid?
Welke term beschrijft het beste het aantal individuen van een bepaalde soort per oppervlakte-eenheid?  Waarom is fotosyntheses zo belangrijk voor het leven op aarde?
Waarom is fotosyntheses zo belangrijk voor het leven op aarde?  Onderzoek toont aan dat wetlands de stikstofvervuiling op landschapsschaal verminderen
Onderzoek toont aan dat wetlands de stikstofvervuiling op landschapsschaal verminderen Ghana moet overgaan van het omgaan met overstromingen naar het zich eraan aanpassen
Ghana moet overgaan van het omgaan met overstromingen naar het zich eraan aanpassen Enorme Antarctische ijsberg kan jarenlang door oceaan drijven
Enorme Antarctische ijsberg kan jarenlang door oceaan drijven
Hoofdlijnen
- Ondanks bosverlies, een beschermd Afrikaans gebied heeft nog steeds potentieel om tienduizenden olifanten te ondersteunen, 1K leeuwen
- Welke koninkrijken vormen bacteriën?
- Wat is de betekenis van wetenschapper?
- Een testcross op een lange erwtenplant produceert alleen nakomelingen. Wat is het genotype van de plant?
- Uit welke xyleemcellen bestaat het grootste deel van hout?
- Produceert het lymfestelsel hormonen en enzymen?
- Waar is de celdeling in de huidweefsel van dieren verantwoordelijk voor?
- Zijn gemeenschappen bestaan uit organismen?
- Welke van de volgende uitdrukkingen is geen functie Mitosis productie gameten groeit vervangingscellen of herstelschade door letsel?
- Draagbare chemiekit maakt het mogelijk om de zoetheid van bushfood ter plaatse te testen

- Machine learning onthult nieuwe kandidaatmaterialen voor biocompatibele elektronica

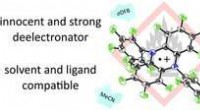
- Chemici produceren nieuwe oxidanten als hulpmiddel voor preparatieve chemie
- Chemicaliën die vaak worden gebruikt in scheikundelaboratoria op middelbare scholen

- Microgelmysteries ontrafelen

 Wat betekent oplossing in de wetenschap voor kinderen?
Wat betekent oplossing in de wetenschap voor kinderen?  Is suiker een chemische vorm van materie met duidelijke vorm en volume?
Is suiker een chemische vorm van materie met duidelijke vorm en volume?  Beschrijf hoe elektrisch potentieel energiekinetisch en werkverandering wanneer twee ladingen van tegengesteld teken bij elkaar worden geplaatst?
Beschrijf hoe elektrisch potentieel energiekinetisch en werkverandering wanneer twee ladingen van tegengesteld teken bij elkaar worden geplaatst?  Hoe de pH te titreren
Hoe de pH te titreren Astrofysici bevestigen hoeksteen van Einsteins relativiteitstheorie
Astrofysici bevestigen hoeksteen van Einsteins relativiteitstheorie Ramplessen:wat je niet weet, kan dodelijk zijn
Ramplessen:wat je niet weet, kan dodelijk zijn  De Tennessee State Bird, Tree and Flower
De Tennessee State Bird, Tree and Flower Fotosynthese en cellulaire ademhaling maken deel uit van welke cyclus?
Fotosynthese en cellulaire ademhaling maken deel uit van welke cyclus?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

