
Wetenschap
Berekening van de molaire massa van ammoniumfosfaat ((NH₄)₃PO₄) - een stapsgewijze handleiding
1. Identificeer de elementen en hun atoommassa's:
* Stikstof (N): 14,01 g/mol
* Waterstof (H): 1,01 g/mol
* Fosfor (P): 30,97 g/mol
* Zuurstof (O): 16,00 g/mol
2. Bereken het aantal atomen van elk element:
* Stikstof (N): 3 atomen
* Waterstof (H): 12 atomen (3 x 4)
* Fosfor (P): 1 atoom
* Zuurstof (O): 4 atomen
3. Vermenigvuldig de atoommassa met het aantal atomen:
* Stikstof: 14,01 g/mol * 3 =42,03 g/mol
* Waterstof: 1,01 g/mol * 12 =12,12 g/mol
* Fosfor: 30,97 g/mol * 1 =30,97 g/mol
* Zuurstof: 16,00 g/mol * 4 =64,00 g/mol
4. Tel de molmassa's van elk element op:
42,03 g/mol + 12,12 g/mol + 30,97 g/mol + 64,00 g/mol =149,12 g/mol
Daarom is de molaire massa van ammoniumfosfaat ((NH₄)₃PO₄) 149,12 g/mol.
 Welke minerale zouten bevatten fosfor?
Welke minerale zouten bevatten fosfor?  Wat is de molariteit van ammoniakoplossing als pH 11,6 en KB 1,8x10-5?
Wat is de molariteit van ammoniakoplossing als pH 11,6 en KB 1,8x10-5?  Hoe u een team van 'passend sceptische' accountants van financiële overzichten kunt samenstellen
Hoe u een team van 'passend sceptische' accountants van financiële overzichten kunt samenstellen  Ei-osmose-experimenten met gedestilleerd water en zout water
Ei-osmose-experimenten met gedestilleerd water en zout water Wat een chemische reactie die energie van de reactanten naar de omgeving overbrengt, wordt elastisch genoemd.
Wat een chemische reactie die energie van de reactanten naar de omgeving overbrengt, wordt elastisch genoemd.
 Het ontrafelen van de mysteries van opeenvolgende atmosferische riviergebeurtenissen
Het ontrafelen van de mysteries van opeenvolgende atmosferische riviergebeurtenissen  Hoe germaneren planten?
Hoe germaneren planten?  Economische kosten van klimaatverandering kunnen zes keer hoger zijn dan eerder werd gedacht
Economische kosten van klimaatverandering kunnen zes keer hoger zijn dan eerder werd gedacht De gevolgen van klimaatverandering projecteren
De gevolgen van klimaatverandering projecteren Om een bloeiende cafécultuur in stand te houden, we moeten de wegwerpbeker weggooien.
Om een bloeiende cafécultuur in stand te houden, we moeten de wegwerpbeker weggooien.
Hoofdlijnen
- Waarom is het domein genaamd Archaea?
- Hebben dierencellen celwanden?
- Het belang van samengestelde microscopen
- Welke niveaus van biologische organisatie zijn het meest inclusief?
- Nieuw geïdentificeerde genen kunnen gewassen helpen beschermen tegen overstromingen
- Waarom wordt penicillium geclassificeerd als deuteromycota?
- Wat is het evenement dat de ontwikkeling en de oprichting van microbiologie als wetenschap veroorzaakte?
- Wat waren de eerste kennis van levende organismen op aarde en wanneer verschenen ze?
- Welke vier lichaamssystemen zijn betrokken bij het verkrijgen van zuurstof naar uw cel?
- Onderzoekers ontwikkelen draagbaar apparaat dat in 10 minuten 3D-afbeeldingen van de huid maakt

- Ongebruikelijke nanodeeltjes kunnen de zoektocht naar een kwantumcomputer ten goede komen
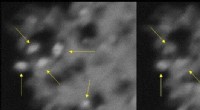
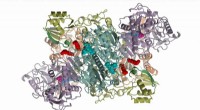
- Moleculaire machinerie die krachtige antibiotica maakt onthuld na tientallen jaren van onderzoek
- Onderzoeksteam ontwikkelt materiaal om olie en water te scheiden voor milieusanering en afvalwaterzuivering

- Molecuuleigenschappen veranderen door licht

 Is het nauwkeurig om natriumchloride te beschrijven als bestaande uit individuele deeltjes die elk één kation en chlooranion vormden?
Is het nauwkeurig om natriumchloride te beschrijven als bestaande uit individuele deeltjes die elk één kation en chlooranion vormden?  Wat is de atomaire structuur van slim materiaal?
Wat is de atomaire structuur van slim materiaal?  Waarom waren wetenschappers het niet eens met de theorie over hoe de continenten bewogen?
Waarom waren wetenschappers het niet eens met de theorie over hoe de continenten bewogen?  Aarde warmt sneller op dan gedacht, nieuwe klimaatmodellen tonen
Aarde warmt sneller op dan gedacht, nieuwe klimaatmodellen tonen Welke organisims zitten er in een vijver?
Welke organisims zitten er in een vijver?  Wat zijn de factoren die een chemische verandering bepalen?
Wat zijn de factoren die een chemische verandering bepalen?  Het trillen van eekhoornstaarten begrijpen:waarom ze het doen en wat het aangeeft
Het trillen van eekhoornstaarten begrijpen:waarom ze het doen en wat het aangeeft  Als u online met korting koopt, betaalt u dan echt meer?
Als u online met korting koopt, betaalt u dan echt meer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

