
Wetenschap
Methanol versus methaanthiol:kookpuntverschillen begrijpen
* Waterstofbinding in methanol (CH3OH): Methanol heeft een waterstofatoom gebonden aan een zuurstofatoom (O-H). Dit maakt waterstofbinding mogelijk, een sterke intermoleculaire kracht die voortkomt uit de aantrekkingskracht tussen een gedeeltelijk positief waterstofatoom en een gedeeltelijk negatief zuurstofatoom op aangrenzende moleculen.
* Dipool-dipoolinteracties in methaanthiol (CH3SH): Methaanthiol heeft een zwavelatoom gebonden aan een waterstofatoom (S-H). Hoewel de S-H-binding polair is, is deze minder polair dan de O-H-binding in methanol. Daarom ervaart methaanthiol zwakkere dipool-dipoolinteracties.
* Londense verspreidingstroepen: Zowel methanol als methaanthiol ondervinden Londense dispersiekrachten, dit zijn zwakke intermoleculaire krachten die voortkomen uit tijdelijke fluctuaties in de elektronenverdeling. Deze krachten zijn echter over het algemeen zwakker dan waterstofbruggen of dipool-dipoolinteracties.
Samengevat: De sterke waterstofbindingsinteracties van methanol zijn aanzienlijk sterker dan de zwakkere dipool-dipoolinteracties in methaanthiol. Deze sterkere intermoleculaire krachten in methanol vereisen meer energie om te overwinnen, wat resulteert in een hoger kookpunt.
 Tropische bosreservaten vertragen de opwarming van de aarde
Tropische bosreservaten vertragen de opwarming van de aarde Wat zijn de meeste soorten vandaag?
Wat zijn de meeste soorten vandaag?  Clean Water Act vermindert de vervuiling in de waterwegen van de VS drastisch
Clean Water Act vermindert de vervuiling in de waterwegen van de VS drastisch Voorbeelden van interactie tussen menselijke omgeving in Colorado?
Voorbeelden van interactie tussen menselijke omgeving in Colorado?  Beschrijf twee manieren waarop mensen het ecosysteem beïnvloeden?
Beschrijf twee manieren waarop mensen het ecosysteem beïnvloeden?
Hoofdlijnen
- Wat converteert de info over mRNA in een reeks aminozuren die eiwit vormen?
- Wat is de specifieke functie van ATP in fotosynthese?
- Zou de ontdekking van een sleutelgensysteem de laatste zucht van koralen kunnen verstikken?
- Hoe worden eiwitten gevormd in een organisme?
- De locaties A P en E worden bezet door aminozuren die worden geassembleerd in een keten van polypeptide waar ze deel van uitmaken?
- Wat dient als de kern voor amoebas en protozoën?
- Een beetje stress is goed voor de gezondheid van de cellen en een lang leven
- DNA draagt genetische informatie in zijn?
- Wat zorgen voor koolhydraten voor de cel?
- Afgedankte apparaten smelten terwijl duurzame behoeften opwarmen

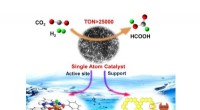
- Katalysator met één atoom gebaseerd op homogeen katalyse-prototype voor CO2-transformatie
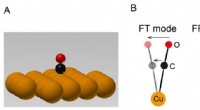
- Opheldering van trillingsenergie van een enkel molecuul in een extern krachtveld
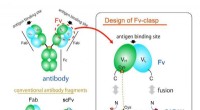
- Nieuw klein antilichaamfragment - een waardevol hulpmiddel bij kristallografie
- Baanbrekende techniek maakt de weg vrij voor snelle en goedkope fabricage van snelle medische diagnostische hulpmiddelen

 Hoe je winnaar kunt worden in het evolutiespel
Hoe je winnaar kunt worden in het evolutiespel  Als een van de twee op elkaar inwerkende ladingen wordt verdubbeld, wordt de kracht tussen Will verdubbeld.
Als een van de twee op elkaar inwerkende ladingen wordt verdubbeld, wordt de kracht tussen Will verdubbeld.  Hoeveel protonen, nuetronen en elektronen heeft Xenon?
Hoeveel protonen, nuetronen en elektronen heeft Xenon?  Wat is urethaan?
Wat is urethaan?  De eerste keer filmen van kwantitatieve metingen
De eerste keer filmen van kwantitatieve metingen Wat is de verandering van een stof van de ene fysieke toestand naar de andere?
Wat is de verandering van een stof van de ene fysieke toestand naar de andere?  Zijn bacteriecellen prokaryotisch of eukaryotisch en waarom?
Zijn bacteriecellen prokaryotisch of eukaryotisch en waarom?  Beschrijf de beweging van korst bij een hotspot?
Beschrijf de beweging van korst bij een hotspot?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

