
Wetenschap
Is chloor meer elektronegatief dan zuurstof?
Nee, zuurstof is meer elektronegatief dan chloor .
Dit is waarom:
* elektronegativiteit is het vermogen van een atoom om elektronen naar zichzelf aan te trekken in een chemische binding.
* Zuurstof heeft een hogere elektronegativiteitswaarde (3,44) dan chloor (3.16) op de Pauling -schaal. Dit betekent dat zuurstof een sterkere trek aan elektronen heeft in een binding in vergelijking met chloor.
Hier is een eenvoudige analogie: Denk aan een touwtrekken. Zuurstof is een sterkere concurrent en zou eerder het "elektronentouw" naar zichzelf trekken.
 Afbeelding:verkeersopstopping Suezkanaal gezien vanuit de ruimte
Afbeelding:verkeersopstopping Suezkanaal gezien vanuit de ruimte NASA-NOAA-satelliet vangt het einde van de post-tropische storm Arthurs
NASA-NOAA-satelliet vangt het einde van de post-tropische storm Arthurs Een manier om groene infrastructuur in uw stad te promoten
Een manier om groene infrastructuur in uw stad te promoten De werelden van ontoegankelijkheid zijn, nou ja, behoorlijk ontoegankelijk
De werelden van ontoegankelijkheid zijn, nou ja, behoorlijk ontoegankelijk De plannen voor het noordpoolgebied van Rusland dragen bij aan de klimaatproblemen van ijsberen
De plannen voor het noordpoolgebied van Rusland dragen bij aan de klimaatproblemen van ijsberen
Hoofdlijnen
- Nieuwe plantibodies zijn veelbelovend om citrus te beschermen tegen vergroeningsziekten
- Biologen ontdekken hoe 'stille' mutaties de eiwitproductie beïnvloeden
- Waar neuroncellichamen zijn gevestigd?
- Hoe zou u de kenmerken van de wetenschap beschrijven-?
- Wat zorgt ervoor dat moleculen van een bepaald eiwit altijd in dezelfde vorm vouwen?
- Ananas mint genetische blauwdruk:een uitgebreide genoomassemblage
- Heeft een bacteriecel membraan?
- In welk bioom werken ontleders het meest efficiënt?
- Wat zijn de verschillende takken in de wetenschap?
- Wetenschappers ontdekken aanpak om inerte gassen te activeren

- Eencellige test kan precies onthullen hoe medicijnen kankercellen doden

- Video:De chemie van gebakken kip

- Neutronen optimaliseren hoogrendementskatalysator voor groenere benadering van biobrandstofsynthese
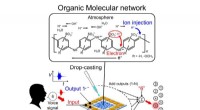
- Intelligentie die voortkomt uit willekeurige polymeernetwerken
 Wat voor soort licht verzamelt de Hubble -telescoop?
Wat voor soort licht verzamelt de Hubble -telescoop?  Waarom wordt het volume gas kleiner als het is gekoeld?
Waarom wordt het volume gas kleiner als het is gekoeld?  Hoe blijven Lo Europa Ganymede en Callisto in een baan om Jupiter?
Hoe blijven Lo Europa Ganymede en Callisto in een baan om Jupiter?  Nieuwe toolkit biedt mobiele productmarkten een routekaart naar succes
Nieuwe toolkit biedt mobiele productmarkten een routekaart naar succes De remmen op de productie van plantaardige olie verwijderen
De remmen op de productie van plantaardige olie verwijderen Welke energiebron kan niet worden vervangen?
Welke energiebron kan niet worden vervangen?  Wat is de chemische structuur van protaminesulfaat?
Wat is de chemische structuur van protaminesulfaat?  Aankomst gezichtsherkenning op luchthavens luidt het biometrische tijdperk in
Aankomst gezichtsherkenning op luchthavens luidt het biometrische tijdperk in
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

