
Wetenschap
Chemische vergelijkingen in evenwicht brengen:ijzersulfaat en natriumhydroxide
1. Identificeer de reactanten en producten:
* Reactanten: IJzersulfaat (FeSO₄) en natriumhydroxide (NaOH)
* Producten: IJzerhydroxide (Fe(OH)₂) en natriumsulfaat (Na₂SO₄)
2. Schrijf de onevenwichtige vergelijking:
FeSO₄(aq) + NaOH(aq) → Fe(OH)₂(s) + Na₂SO₄(aq)
3. Balance the equation:
Om de vergelijking in evenwicht te brengen, moeten we ervoor zorgen dat het aantal atomen van elk element aan beide kanten hetzelfde is:
FeSO₄(aq) + 2 NaOH(aq) → Fe(OH)₂(s) + Na₂SO₄(aq)
De uitgebalanceerde moleculaire vergelijking is:
FeSO₄(aq) + 2NaOH(aq) → Fe(OH)₂(s) + Na₂SO₄(aq)
Uitleg:
* (aq) geeft aan dat de stof is opgelost in water (waterige oplossing).
* (s) geeft aan dat de stof een vast neerslag is.
Deze reactie produceert een groen neerslag van ijzerhydroxide, dat onoplosbaar is in water.
 Wijngaardtoerisme is een grote bron van koolstofemissies; het kopen van meer wijn ter plaatse kan dit helpen verminderen
Wijngaardtoerisme is een grote bron van koolstofemissies; het kopen van meer wijn ter plaatse kan dit helpen verminderen Walvisvangst:waarom de praktijk niet zal verdwijnen
Walvisvangst:waarom de praktijk niet zal verdwijnen  Kunnen we de oogst van houtachtige biomassa uit Europese bossen vergroten?
Kunnen we de oogst van houtachtige biomassa uit Europese bossen vergroten?  Online calculator laat zien hoe bomen de luchtkwaliteit kunnen verbeteren en de gezondheidskosten kunnen verlagen
Online calculator laat zien hoe bomen de luchtkwaliteit kunnen verbeteren en de gezondheidskosten kunnen verlagen  Giftig en opraken:Pakistaanse watercrisis
Giftig en opraken:Pakistaanse watercrisis
Hoofdlijnen
- Welk organisme produceert hun eigen voedsel en levert de andere organismen in een ecosysteem met energievoedingsstoffen?
- Hoeveel cellen hebben levende wezens?
- Hoe presenteren wetenschappers wetenschappelijke gegevens?
- Genetisch materiaal in levend organisme bestaat uit organische moleculen die worden genoemd?
- Wat is het meeste type cel in het lichaam?
- Wanneer ontwikkelen baby's liefde voor spraak?
- Hoe produceren verschillende restrictie -enzymen DNA -fragmenten uit het molecuul?
- Plasmamembraan: definitie, structuur en functie (met diagram)
- Hoe mRNA en tRNA samenwerken om eiwitten te bouwen
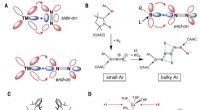
- Onderzoekers vinden verrassende bindingen van het overgangsmetaaltype tijdens het bouwen van nieuwe calcium(I)-complexen
- Nieuw bioremediatiemateriaal kan chemicaliën voor altijd reinigen

- Nieuw polymeer geeft moleculaire lading vrij als reactie op kracht

- Waarom u uw overgebleven koffiedik moet bewaren:een door de wetenschap ondersteunde gids

- Nieuw maskermateriaal kan nanodeeltjes van virusgrootte verwijderen

 Wat zijn de kleine haarachtige structuren voor beweging of het detecteren van dingen in een cel?
Wat zijn de kleine haarachtige structuren voor beweging of het detecteren van dingen in een cel?  Redox-titratie:de principes en toepassingen begrijpen
Redox-titratie:de principes en toepassingen begrijpen  Wat bestaat uit een ster en de objecten eromheen?
Wat bestaat uit een ster en de objecten eromheen?  Wat als koolstofgrensbelastingen ook van toepassing zijn op alle koolstof en fossiele brandstoffen?
Wat als koolstofgrensbelastingen ook van toepassing zijn op alle koolstof en fossiele brandstoffen?  Wat biedt het energie dat de vrije elektronen in een geleider duwt?
Wat biedt het energie dat de vrije elektronen in een geleider duwt?  Achtervolgende reuzen:aanwijzingen voor hoe mensen en giraffen samen kunnen gedijen
Achtervolgende reuzen:aanwijzingen voor hoe mensen en giraffen samen kunnen gedijen  Moleculaire atlas van een Australisch drakenbrein werpt nieuw licht op meer dan 300 miljoen jaar hersenevolutie
Moleculaire atlas van een Australisch drakenbrein werpt nieuw licht op meer dan 300 miljoen jaar hersenevolutie Hoe kun je zien of een nanodeeltje leeft?
Hoe kun je zien of een nanodeeltje leeft?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

