
Wetenschap
Redox-titratie:de principes en toepassingen begrijpen
Redox-titratie:een dans van elektronen
Redox-titratie is, net als zijn zuur-base-tegenhanger, een krachtige analytische techniek die wordt gebruikt om de concentratie van een onbekende oplossing te bepalen. Maar in plaats van zich te concentreren op de overdracht van protonen, draait het om de overdracht van elektronen tussen de analyt (onbekende oplossing) en een titrant (oplossing met een bekende concentratie).
Hier is de uitsplitsing:
1. Het principe:
- Redoxreactie: De kern van redoxtitratie ligt in een redoxreactie tussen de analyt en de titrant. Deze reactie omvat de overdracht van elektronen, waarbij de ene soort wordt geoxideerd (elektronen verliest) en de andere wordt gereduceerd (elektronen wint).
- Equivalentiepunt: De titratie gaat door totdat het equivalentiepunt is bereikt. Dit is het punt waarop de analyt en de titrant volledig hebben gereageerd, wat betekent dat al het oxidatiemiddel is gereduceerd en al het reductiemiddel is geoxideerd.
- Indicator: Om het equivalentiepunt visueel te identificeren, wordt vaak een redoxindicator gebruikt. Deze indicator verandert van kleur bij een specifiek potentieel, wat de voltooiing van de reactie aangeeft.
2. Hoe het werkt:
- Titrant: De titrant bevat een bekende concentratie van een oxidatie- of reductiemiddel.
- Analiet: De onbekende oplossing bevat de analyt waarvan u de concentratie wilt bepalen.
- Reactie: Wanneer de titrant druppelsgewijs aan de analyt wordt toegevoegd, vindt er een redoxreactie plaats.
- Equivalentiepunt: Het equivalentiepunt wordt bereikt wanneer de stoichiometrische hoeveelheid titrant is toegevoegd om volledig te reageren met de analyt.
- Berekeningen: Het op het equivalentiepunt gebruikte volume titrant wordt vervolgens gebruikt om de concentratie van de analyt te berekenen met behulp van de bekende concentratie van de titrant en de stoichiometrie van de reactie.
3. Toepassingen:
Redox-titratie wordt veel gebruikt op verschillende gebieden, waaronder:
- Milieuchemie: Bepalen van de concentratie van verontreinigende stoffen zoals zware metalen en oxidatiemiddelen.
- Voedselchemie: Analyse van het vitamine C-gehalte in groenten en fruit.
- Farmaceutische industrie: Bepalen van de zuiverheid en potentie van medicijnen en medicijnen.
- Industriële chemie: Meten van de concentratie van metalen, halogeniden en andere stoffen in diverse industriële processen.
4. Voorbeelden:
- Bepaling van de concentratie ijzer(II)-ionen met behulp van kaliumpermanganaat als titrant. Permanganaationen (MnO4-) werken als oxidatiemiddel en zetten ijzer(II)-ionen om in ijzer(III)-ionen. Het eindpunt wordt aangegeven door de aanhoudende roze kleur van de permanganaationen.
- Bepaling van de jodiumconcentratie met behulp van natriumthiosulfaat als titrant. Jodium werkt als oxidatiemiddel en natriumthiosulfaat als reductiemiddel. Het eindpunt wordt aangegeven door het verdwijnen van de bruine kleur van jodium.
In wezen is redoxtitratie een krachtig hulpmiddel voor het analyseren van de concentratie van stoffen door gebruik te maken van de kracht van elektronenoverdrachtsreacties.
 Vergeet slimme steden (voor een minuut), we moeten het hebben over slimme boerderijen
Vergeet slimme steden (voor een minuut), we moeten het hebben over slimme boerderijen Kunnen downloads de impact van wetenschappelijke artikelen voorspellen?
Kunnen downloads de impact van wetenschappelijke artikelen voorspellen?  Milieuproblemen die batterijen veroorzaken
Milieuproblemen die batterijen veroorzaken Natuurlijke cycli in de Golf van Alaska accentueren verzuring van de oceaan
Natuurlijke cycli in de Golf van Alaska accentueren verzuring van de oceaan Scott Pruitts benadering van vervuilingsbeheersing zal de lucht vuiler maken en Amerikanen minder gezond
Scott Pruitts benadering van vervuilingsbeheersing zal de lucht vuiler maken en Amerikanen minder gezond
Hoofdlijnen
- Wat is de opeenstapeling van verschillen tussen groepen die leiden tot de vorming van nieuwe soorten?
- De drie stappen van een monohybride kruis begrijpen
- Hoe cellen zichzelf meten
- Wat is de biologische rol van maltose?
- Wat zijn de SAB-branches van de evolutiebiologie?
- Orgelsystemen kunnen uit cellen of weefsels worden samengesteld, maar niet beide?
- Biobrandstoffen als invasieve soort?
- Waarom zijn het allemaal levende wezens afkomstig van een gewone of universele voorouder?
- Welke groeimedia geven een rode kolonie van Escherechia coli?
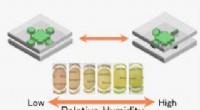
- Functionele films gemaakt van milieuvriendelijke kleimineralen en kleurstoffen
- Waarom drinkwater moet worden gecontroleerd op hiv-medicijnen

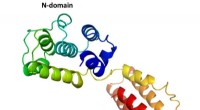
- Wetenschappers halen structuur van zalmvirus binnen
- Cementvrij beton verslaat corrosie en geeft fatbergs de flush

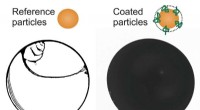
- Het modificeren van oppervlakken met polymeerketens bevordert een gelijkmatige droging van deeltjesbevattende vloeistoffen
 Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels
Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels Wat zijn 3 manieren waarop de energie in de atmosfeer wordt overgedragen?
Wat zijn 3 manieren waarop de energie in de atmosfeer wordt overgedragen?  Hoe de beweging voor desinvestering van fossiele brandstoffen kan worden opgelost
Hoe de beweging voor desinvestering van fossiele brandstoffen kan worden opgelost  Welke krachten handelen op objecten in rust?
Welke krachten handelen op objecten in rust?  Stap-voor-stap handleiding:Zilveroxide synthetiseren uit zilvernitraat
Stap-voor-stap handleiding:Zilveroxide synthetiseren uit zilvernitraat  Als de golflengte van een radioshoton van een AM -station 220 m is, wat zijn energie?
Als de golflengte van een radioshoton van een AM -station 220 m is, wat zijn energie?  Mannen trollen meer op Facebook dan vrouwen vanwege narcisme, studie suggereert:
Mannen trollen meer op Facebook dan vrouwen vanwege narcisme, studie suggereert: Hoe regenbogen werken
Hoe regenbogen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

