
Wetenschap
HCl- en ammoniakgasreactie:volumeveranderingen uitgelegd
Reactie:
Ammoniakgas reageert met zoutzuur in een neutralisatiereactie en vormt ammoniumchloride (NH₄Cl), een zout en water (H₂O):
```
NH₃(g) + HCl(aq) → NH₄Cl(aq)
```
Volumewijzigingen:
* Initieel volume: Je begint met een bepaald volume HCl-oplossing.
* Ammoniak toevoegen: Terwijl ammoniakgas wordt toegevoegd, lost het op in de oplossing en reageert het met HCl.
* Volumereductie: Bij de reactie ontstaat ammoniumchloride, een zout dat in de oplossing oplost. Het volume van de oplossing zal echter iets afnemen omdat bij de reactie ook water ontstaat. Deze volumedaling is doorgaans verwaarloosbaar.
* Netto-effect: Het netto-effect op het volume is een lichte reductie door watervorming, maar deze verandering is vaak te klein om op te merken.
Belangrijke overwegingen:
* Concentratie: De concentratie van de HCl-oplossing en de toegevoegde hoeveelheid ammoniakgas bepalen de omvang van de reactie.
* Exotherme reactie: De reactie tussen ammoniak en zoutzuur is exotherm, wat betekent dat er warmte vrijkomt. Deze hitte kan een lichte uitzetting van de oplossing veroorzaken als deze niet onder controle wordt gehouden.
Samengevat: Het toevoegen van ammoniakgas aan zoutzuur resulteert in een neutralisatiereactie, waarbij ammoniumchloride en water worden geproduceerd. Hoewel er een lichte volumevermindering optreedt als gevolg van watervorming, is de totale verandering in volume gewoonlijk verwaarloosbaar.
 Wat is het verschil tussen avicel pH 101 en 112?
Wat is het verschil tussen avicel pH 101 en 112?  Welk element is een vloeistof bij kamertemperatuur en heksengastemperatuur?
Welk element is een vloeistof bij kamertemperatuur en heksengastemperatuur?  Kan verdamping worden gebruikt om vaste stoffen te verwijderen?
Kan verdamping worden gebruikt om vaste stoffen te verwijderen?  Welke elementen van het periodiek systeem zijn vaste stoffen of vloeistoffen en welke gassen?
Welke elementen van het periodiek systeem zijn vaste stoffen of vloeistoffen en welke gassen?  Tekeneiwit helpt antibiotica MRSA-superbug te bestrijden
Tekeneiwit helpt antibiotica MRSA-superbug te bestrijden
 Hoe bepaal ik of een inktvis mannelijk of vrouwelijk is?
Hoe bepaal ik of een inktvis mannelijk of vrouwelijk is?  Wie zei dat de natuur waarheid geluk en deugd samenbindt als door een onoplosbare keten?
Wie zei dat de natuur waarheid geluk en deugd samenbindt als door een onoplosbare keten?  Veranderende levensstijl als reactie op de effecten van klimaatverandering
Veranderende levensstijl als reactie op de effecten van klimaatverandering  Kankertumoren kunnen helpen het mysterie van de Cambrische explosie te ontrafelen
Kankertumoren kunnen helpen het mysterie van de Cambrische explosie te ontrafelen Snowkyo 2020:organisatoren in Tokio testen nepsneeuw om Olympische Spelen te koelen
Snowkyo 2020:organisatoren in Tokio testen nepsneeuw om Olympische Spelen te koelen
Hoofdlijnen
- Wat is de structuur van een nucleotide in DNA -molecuul?
- Wat hebben wetenschapper nodig voor de hypothese?
- Welke bacteriën hebben geen celwand?
- Wat zijn de belangrijkste organen voor het skeletsysteem?
- Wat is een pseudogeen?
- Welk orgaan is verantwoordelijk voor het produceren van de hormooninsuline om de bloedsuikerspiegel in het menselijk lichaam te verlagen?
- Hoe verkrijgen bloeiende planten voedsel?
- Weefsels zijn georganiseerd in functionele eenheden die worden genoemd?
- Kan eten mensen gelukkig maken?
- Levensmiddelentechnologie:Insectenmeel

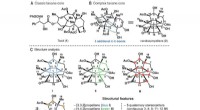
- Licht als hulpmiddel voor de synthese van complexe moleculen

- Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren
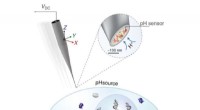
- Verbeterde pH-sondes kunnen helpen bij kankerbehandelingen
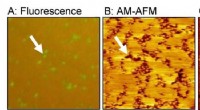
- Assemblage van fluctuerende moleculen in kunstmatig celmembraan
 Door virussen getroffen luchtvaartmaatschappijen worden geconfronteerd met reddingsoperaties of faillissement
Door virussen getroffen luchtvaartmaatschappijen worden geconfronteerd met reddingsoperaties of faillissement Drie manieren om een nagel te magnetiseren
Drie manieren om een nagel te magnetiseren Wat was de snelste reis naar de maan?
Wat was de snelste reis naar de maan?  Wanneer energieoverdracht naar lucht wat gebeurt er de luchtdeeltjes?
Wanneer energieoverdracht naar lucht wat gebeurt er de luchtdeeltjes?  Hoe veranderen de temperaturen van noord naar zuid op een kaart?
Hoe veranderen de temperaturen van noord naar zuid op een kaart?  Beweegt de zon zich rond de aarde?
Beweegt de zon zich rond de aarde?  Theorie helpt bij de analyse van nucleair materiaal
Theorie helpt bij de analyse van nucleair materiaal Wat probeerde Ptolemy in zijn model uit te leggen door de planeten op kleinere cirkels te laten bewegen die grotere kringen zijn?
Wat probeerde Ptolemy in zijn model uit te leggen door de planeten op kleinere cirkels te laten bewegen die grotere kringen zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

