
Wetenschap
Vorming van natrium-chloorbinding:elektronenoverdracht en creatie van NaCl
* Natrium (Na): Natrium heeft één elektron in de buitenste schil. Het wil dit elektron kwijtraken om een stabiele elektronenconfiguratie zoals het edelgas Neon (Ne) te bereiken.
* Chloor (Cl): Chloor heeft zeven elektronen in de buitenste schil. Het wil één elektron winnen om een stabiele elektronenconfiguratie te bereiken, zoals het edelgas Argon (Ar).
De reactie:
1. Elektronenoverdracht: Het natriumatoom verliest zijn buitenste elektron en wordt een positief geladen natriumion (Na+). Dit elektron wordt vervolgens overgebracht naar het chlooratoom, dat een negatief geladen chloride-ion (Cl-) wordt.
2. Ionische binding: De tegengesteld geladen ionen (Na+ en Cl-) trekken elkaar elektrostatisch aan, waardoor een ionische binding ontstaat. Deze sterke elektrostatische aantrekkingskracht houdt de ionen bij elkaar in een kristalroosterstructuur.
Belangrijkste punten:
* Octetregel: Zowel natrium als chloor bereiken een stabiele elektronenconfiguratie door de octetregel te volgen, die stelt dat atomen de neiging hebben elektronen te winnen, te verliezen of te delen om acht elektronen in hun buitenste schil te hebben.
* Ionische verbinding: De resulterende verbinding, natriumchloride, is een ionische verbinding. Ionische verbindingen worden gevormd door de elektrostatische aantrekking tussen positief en negatief geladen ionen.
Samengevat: De reactie tussen natrium en chloor omvat de overdracht van een elektron van natrium naar chloor, waarbij ionen worden gevormd die vervolgens bij elkaar worden gehouden door een ionische binding.
 Wat is voorbeeld van een van de eerste landplanten die moeten evolueren?
Wat is voorbeeld van een van de eerste landplanten die moeten evolueren?  Beslissingen over watergebruik moeten de veranderende trends in het lokale hydroklimaat weerspiegelen
Beslissingen over watergebruik moeten de veranderende trends in het lokale hydroklimaat weerspiegelen Wetenschappers voorspellen gemiddelde dode zone, maar 3x langetermijndoel
Wetenschappers voorspellen gemiddelde dode zone, maar 3x langetermijndoel De Arabische plaat houdt stand
De Arabische plaat houdt stand Noordelijke veengebieden zullen een deel van hun koolstofdioxideopslagcapaciteit verliezen onder een warmer klimaat
Noordelijke veengebieden zullen een deel van hun koolstofdioxideopslagcapaciteit verliezen onder een warmer klimaat
Hoofdlijnen
- Wat zijn vier eigenschappen die worden gecontroleerd door erfelijkheid?
- Hoe heten de anucleaire cellen die zuurstofcellen transporteren?
- Kenmerken van een bacteriële cel
- De belangrijkste rol bij het bepalen van de verdeling van biomen komt vandaan?
- Wat is een FLASK-definitie?
- Hoe overleven organismen in een gesloten ecosysteem?
- Wat ontvangt eiwitten en andere nieuw gevormde materialen verdelen ze over delen van de cel?
- Wat is een organisme in actie en verandert het gedrag dat optreedt als gevolg van een stimulus?
- Wat betekent abnormaal resultaat in de wetenschap?
- Dynamisch 3D-printproces met lichtgestuurde draai
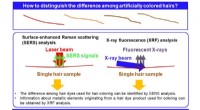
- Binnen een haarbreedte - forensische identificatie van enkel geverfde haarstreng nu mogelijk
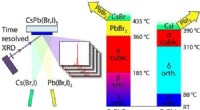
- Krachtige zonnecellen:natuurkundigen kweken stabiele perovskietlagen
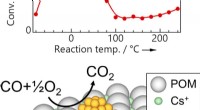
- Ultra-efficiënte verwijdering van koolmonoxide met behulp van gouden nanodeeltjes op een moleculaire drager
- Nieuw proces versnelt medicamenteuze behandelingen voor virale infecties en kanker

 Hoe signaalmoleculen voor de vorming van verschillende celtypen worden aangestuurd
Hoe signaalmoleculen voor de vorming van verschillende celtypen worden aangestuurd  Welk type energie komt vrij in een gasoven?
Welk type energie komt vrij in een gasoven?  Mechanische golven worden volgens wat geclassificeerd?
Mechanische golven worden volgens wat geclassificeerd?  Serendipiteitsexperiment in de achtertuin werpt licht op de productie van polymeren
Serendipiteitsexperiment in de achtertuin werpt licht op de productie van polymeren Een schapenmelksmoothie serveren
Een schapenmelksmoothie serveren Taallessen voor politie zouden meer Dark Web-pedofielen kunnen vangen
Taallessen voor politie zouden meer Dark Web-pedofielen kunnen vangen Hoe glasdiodes te identificeren en te verifiëren:een praktische gids voor ingenieurs
Hoe glasdiodes te identificeren en te verifiëren:een praktische gids voor ingenieurs  Project maakt gebruik van crowd computing om waterfiltratie te verbeteren
Project maakt gebruik van crowd computing om waterfiltratie te verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

