
Wetenschap
Stoichiometrieberekening:bepaling van de productopbrengst in MgCl₂ + KOH-reactie
De evenwichtige chemische vergelijking
De reactie die u heeft gegeven luidt:
MgCl₂ + 2KOH → Mg(OH)₂ + 2KCl
Deze vergelijking vertelt ons:
* 1 mol MgCl₂ reageert met 2 mol KOH
* Dit levert 1 mol Mg(OH)₂ en 2 mol KCl op
Bepalen van de beperkende reagens
Om erachter te komen hoeveel product er wordt gemaakt, moeten we de beperkende reactant identificeren . Dit is de reactant die als eerste wordt opgebruikt en beperkt daarom de hoeveelheid product die kan worden gevormd.
1. Molen MgCl₂: U zei dat er 3 mol MgCl₂ zijn toegevoegd.
2. Mollen KOH: U zei dat er 4 mol KOH zijn toegevoegd.
3. molverhouding: Uit de uitgebalanceerde vergelijking weten we dat 1 mol MgCl₂ reageert met 2 mol KOH.
4. Vergelijken:
* Voor 3 mol MgCl₂ zijn 3 mol * 2 =6 mol KOH nodig om volledig te reageren.
*Aangezien we slechts 4 mol KOH hebben, is KOH de beperkende reactant.
De hoeveelheid product berekenen
Omdat KOH de beperkende reactant is, gebruiken we de hoeveelheid om te bepalen hoeveel product er wordt gevormd.
1. Mg(OH)₂: De uitgebalanceerde vergelijking laat een verhouding van 2:1 zien tussen KOH en Mg(OH)₂ (2 mol KOH levert 1 mol Mg(OH)₂ op).
* Met 4 mol KOH kunnen we 4 mol / 2 =2 mol Mg(OH)₂ produceren.
2. KCl: De uitgebalanceerde vergelijking toont een verhouding van 2:2 tussen KOH en KCl (2 mol KOH produceert 2 mol KCl).
* Met 4 mol KOH kunnen we 4 mol produceren * (2/2) =4 mol KCl.
Samenvatting
Bij deze reactie met 3 mol MgCl2 en 4 mol KOH is KOH de beperkende reactant. Dit betekent dat wij kunnen produceren:
* 2 mol Mg(OH)₂
* 4 mol KCl
 Wat toont de formule NA2CO3 over compound?
Wat toont de formule NA2CO3 over compound?  Wat dronken ze? Onderzoekers onderzoeken radioactieve crockpots
Wat dronken ze? Onderzoekers onderzoeken radioactieve crockpots  Reageren ammoniumsulfaat en kaliumchloride?
Reageren ammoniumsulfaat en kaliumchloride?  Ionotronische technologie waarvoor geen vloeibare elektrolyten nodig zijn
Ionotronische technologie waarvoor geen vloeibare elektrolyten nodig zijn Ontwikkeling van een nieuwe grootschalige productietechnologie voor sulfide vaste elektrolyten
Ontwikkeling van een nieuwe grootschalige productietechnologie voor sulfide vaste elektrolyten
 Stormen hebben recordaantal bomen geveld in Polen:ambtenaren
Stormen hebben recordaantal bomen geveld in Polen:ambtenaren Uit onderzoek blijkt hoe gewasprijzen en klimaatvariabelen het opbrengstareaal beïnvloeden
Uit onderzoek blijkt hoe gewasprijzen en klimaatvariabelen het opbrengstareaal beïnvloeden  Diversiteit of achterstelling – wat een ‘slechte’ buurt maakt
Diversiteit of achterstelling – wat een ‘slechte’ buurt maakt  Nieuw publiek-privaat onderzoek heft de traditionele koolstofbeprijzing op en biedt een effectievere methode om emissies te beprijzen
Nieuw publiek-privaat onderzoek heft de traditionele koolstofbeprijzing op en biedt een effectievere methode om emissies te beprijzen Atlantic Haven is een proeftuin voor ziekelijke oceanen van planeten
Atlantic Haven is een proeftuin voor ziekelijke oceanen van planeten
Hoofdlijnen
- Samen gekweekte gewassen werken beter samen in slechts twee generaties
- Wat is de relatie tussen cellenweefselsorganen en orgaansystemen?
- Waarom functioneren eiwitten goed, tenzij ze worden ondergedompeld in water?
- Objecten die door mensen worden gemaakt en gebruikt, worden wat genoemd?
- Onderzoekers meten de bereidheid van kleinschalige vissers om vaartuigvolgsystemen te gebruiken
- Wat ons zonnebrand bezorgt, beschermt rivierkreeften tegen bacteriën
- Wat produceert de voorafheid van eiwitten vooraf?
- Wat is de betekenis van reproduceren?
- Hoe een organisme eruit ziet, ongeacht de allelen van het type wordt gerefereerd als wat?
- Snelle en efficiënte scheiding van olie en water bereikt door nieuw ontwikkelde deeltjes

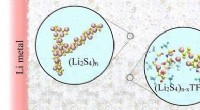
- Optimalisatie van de elektrolyten van lithium-zwavelbatterijen voor een lange levensduur
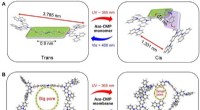
- Microporeuze polymeermembranen voor licht-gated ionentransport
- Kunstbijen uit een snelkookpan?

- Insecten in vriesgebieden hebben een eiwit dat werkt als antivries

 Wat voor solide verandert zijn niet?
Wat voor solide verandert zijn niet?  Waarom lijken sterrenbeelden op verschillende plaatsen te zijn in tijden van het jaar?
Waarom lijken sterrenbeelden op verschillende plaatsen te zijn in tijden van het jaar?  Onderzoekers ontwikkelen recycling voor koolstofvezelcomposieten
Onderzoekers ontwikkelen recycling voor koolstofvezelcomposieten Wat is de op een na moeilijkste rots op aarde?
Wat is de op een na moeilijkste rots op aarde?  "Types of Plant Fossils
"Types of Plant Fossils Piramide pakt gezondheids- en klimaateffecten van voedsel aan
Piramide pakt gezondheids- en klimaateffecten van voedsel aan Hoe berekent u het molecuulgewicht van stikstofoxide?
Hoe berekent u het molecuulgewicht van stikstofoxide?  Weathering Effects
Weathering Effects
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

