
Wetenschap
Zilvernitraat en ijzerreactie:een gedetailleerde uitleg
Reactie:
* Zilvernitraat (AgNO₃) , een kleurloze oplossing, reageert met ijzer (Fe) , een massief metaal.
* Hoe reactiever ijzer het minder reactieve zilver uit de zilvernitraatoplossing verdringt.
* IJzer(II)nitraat (Fe(NO₃)₂) Er wordt een groenachtige oplossing gevormd.
* Zilver (Ag) , een vast metaal, wordt uit de oplossing afgezet als een grijsachtig wit neerslag.
Vergelijking:
2 AgNO₃(aq) + Fe(s) → Fe(NO₃)₂(aq) + 2 Ag(s)
Opmerkingen:
* U zult zien dat zich een grijsachtig wit neerslag vormt op het oppervlak van het ijzermetaal.
* De oplossing verandert van kleurloos in groenachtig.
* Het ijzermetaal begint op te lossen.
Uitleg:
Deze reactie vindt plaats omdat ijzer reactiever is dan zilver op de reactiviteitsreeks van metalen. Dit betekent dat ijzer een sterkere neiging heeft om elektronen te verliezen en positieve ionen te vormen. Bij de reactie verliezen ijzeratomen elektronen om Fe²⁺-ionen te vormen, terwijl zilverionen (Ag⁺) in de oplossing elektronen winnen en zilveratomen worden.
Opmerking:
* De reactie kan worden versneld door de oplossing te verwarmen of door een meer geconcentreerde oplossing van zilvernitraat te gebruiken.
* De reactie kan worden gebruikt om zilvermetaal te produceren uit zilvernitraatoplossingen.
*Deze reactie is ook een goed voorbeeld van een redoxreactie, waarbij elektronen worden overgedragen van ijzer naar zilver.
Hoofdlijnen
- Hoe is een gespecialiseerde rode bloedcel?
- Wat is het verschil tussen natuurbeschermingsbiologie en biotechnologie?
- Wat is de variabele die door wetenschappers wordt bestuurd?
- Dierlijke versus plantaardige cellen:een uitgebreide gids voor celstructuren
- Afrikaanse slaapziekte:hoe de ziekteverwekker tseetseevliegen koloniseert
- Wat hebben wetenschappers geleerd van experimenten die zijn ontworpen om de hypothese te testen dat leven uit niet-levende materialen is ontstaan?
- Wordt de aanwezigheid van endomysium resulterend in skeletspiercellen die elektrisch van elkaar worden geïsoleerd?
- Hoe verhoudt het metabolisme zich tot enzymen?
- Wat zijn de takken van de biologie die zich bezighouden met dieren?
- Move over Rover:er is een nieuwe snuffelende krachtpatser in de buurt

- Een thermisch isolerend composiet van holle silicadeeltjes gemengd met cellulosevezels

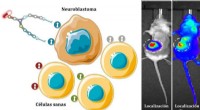
- Synthetische moleculen leveren medicijnen rechtstreeks aan neuroblastoomcellen
- Hoe verandert deze blauwe bloementhee van kleur?

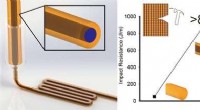
- 3D-printen van plastic onderdelen verbeteren
 Wat wordt gevormd door CuSO4 plus HCl?
Wat wordt gevormd door CuSO4 plus HCl?  Wat gebeurt er met de luchtdeeltjes als er een compressie is?
Wat gebeurt er met de luchtdeeltjes als er een compressie is?  Nieuwe gorilla in Audubon Zoo mag nog even binnen blijven
Nieuwe gorilla in Audubon Zoo mag nog even binnen blijven Wat is het pad van projectiel in vacuüm?
Wat is het pad van projectiel in vacuüm?  El Nino niet verantwoordelijk voor overstromingen in Oost-Afrika:wetenschappers
El Nino niet verantwoordelijk voor overstromingen in Oost-Afrika:wetenschappers  Hoe zijn rotsen gerelateerd aan mineralen?
Hoe zijn rotsen gerelateerd aan mineralen?  Hoe de hoogte van een ruit te vinden
Hoe de hoogte van een ruit te vinden  Welke wetenschapper verklaarde dat al het leven van cellen zijn gemaakt?
Welke wetenschapper verklaarde dat al het leven van cellen zijn gemaakt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


