
Wetenschap
Redoxreacties voorspellen:zilver- en koperioninteracties
De concepten begrijpen
* Redoxreacties: Betrek de overdracht van elektronen. Oxidatie is het verlies van elektronen en reductie is de winst van elektronen.
* Activiteitenreeks: Een lijst met metalen gerangschikt in volgorde van hun reactiviteit, met de meest reactieve bovenaan. Dit helpt voorspellen welk metaal zal worden geoxideerd en welk metaal zal worden gereduceerd.
De concepten toepassen
1. Activiteitenreeks: Zilver (Ag) is minder reactief dan koper (Cu). Dit betekent dat het waarschijnlijker is dat koper elektronen verliest (oxideert) en dat zilver eerder elektronen opneemt (reduceert).
2. Mogelijke reacties: Er zijn twee mogelijke reacties:
* Reactie 1: Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
* Koper (Cu) wordt geoxideerd tot Cu²⁺.
* Zilverionen (Ag⁺) worden gereduceerd tot zilvermetaal (Ag).
* Reactie 2: Ag(s) + Cu²⁺(aq) → Geen reactie
*Deze reactie is onwaarschijnlijk omdat zilver minder reactief is dan koper.
Conclusie
De meest waarschijnlijke redoxreactie is:
Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
Deze reactie zal optreden omdat koper reactiever is dan zilver en daarom waarschijnlijker elektronen aan de zilverionen zal doneren.
 Onderzoekers ontdekken hoe te veel zuurstof cellen en weefsels beschadigt
Onderzoekers ontdekken hoe te veel zuurstof cellen en weefsels beschadigt  Eriochrome Black T Solution Preparation
Eriochrome Black T Solution Preparation  Wat is kleiner een celorganel of een atoom?
Wat is kleiner een celorganel of een atoom?  Bewijs dat een nieuwe cent niet van puur koper is gemaakt. Hij heeft een massa van 2,49 en een volume van 0,349 cm3?
Bewijs dat een nieuwe cent niet van puur koper is gemaakt. Hij heeft een massa van 2,49 en een volume van 0,349 cm3?  Wat is de Lewis Dot van Iron III hydroxide?
Wat is de Lewis Dot van Iron III hydroxide?
 Een opwarmend noordpoolgebied zorgt voor extreme weersomstandigheden op onze breedtegraden
Een opwarmend noordpoolgebied zorgt voor extreme weersomstandigheden op onze breedtegraden Vervuild meer is een arme levensader van Nicaraguanen
Vervuild meer is een arme levensader van Nicaraguanen De opvattingen over klimaatverandering veranderen, zelfs in Texas
De opvattingen over klimaatverandering veranderen, zelfs in Texas Nieuwe studie onthult dat Ulsan jarenlang wordt blootgesteld aan giftig fijnstof
Nieuwe studie onthult dat Ulsan jarenlang wordt blootgesteld aan giftig fijnstof Overstromingen sluiten luchthaven in Indiase toeristische hotspot van Kerala
Overstromingen sluiten luchthaven in Indiase toeristische hotspot van Kerala
Hoofdlijnen
- Hebben mannen en vrouwen verschillende hersenen?
- Wat beïnvloedt de groei van bacteriën?
- Hoeveel genen zijn er in DNA?
- Welke phyla zijn verantwoordelijk voor rode getijden?
- Wat betekent Mienral in wetenschapstermen?
- Welk deel van de bacterie kan het beschermen tegen fagocytose door witte bloedcellen?
- Synapsis vormt een chromosoomcomplex dat bekend staat als A?
- zeehonden, vogels en mensen strijden om vis in de Oostzee
- Wat kunnen haaien ons leren over ons hart?
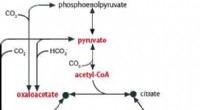
- Ontdekking van een oermetabolisch systeem dat ons een glimp geeft van de oorsprong van het leven op aarde
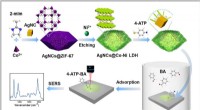
- Nieuwe SERS-sensor helpt bij het detecteren van aldehydegassen
- Nieuwe stof kan je helpen koel te blijven in de zomer, zelfs zonder airco

- Een nieuwe formule voor het creëren van chemische reacties - met koolhydraten

- Nieuw boormateriaal met hoge hardheid gecreëerd door chemische dampafzetting in plasma

 Roterend blauw laserlicht onthult ongekende dynamiek in levende cellen
Roterend blauw laserlicht onthult ongekende dynamiek in levende cellen Hoe schrijf je de formules van aluminiumchloride?
Hoe schrijf je de formules van aluminiumchloride?  Op welke datum publiceerde Ptolemy het astronomische boek Almagest?
Op welke datum publiceerde Ptolemy het astronomische boek Almagest?  Hoelang duren papierplaten ontleden?
Hoelang duren papierplaten ontleden?  Kookt het voedsel gemakkelijk in de snelkookpan omdat de gemiddelde kinetische energie als deeltjes van gas recht evenredig zijn met het temperatuurgas van Kelvin?
Kookt het voedsel gemakkelijk in de snelkookpan omdat de gemiddelde kinetische energie als deeltjes van gas recht evenredig zijn met het temperatuurgas van Kelvin?  Modellen tonen aan dat het warmteverlies van de aarde aan één kant van de planeet groter is
Modellen tonen aan dat het warmteverlies van de aarde aan één kant van de planeet groter is Wanneer bevindt de maan zich het dichtst bij de aarde in haar baan?
Wanneer bevindt de maan zich het dichtst bij de aarde in haar baan?  Waarom blijft de temperatuur van een substantie constant, hoewel energie wordt toegevoegd?
Waarom blijft de temperatuur van een substantie constant, hoewel energie wordt toegevoegd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

