
Wetenschap
Redoxreacties voorspellen:zilver en koper in ionische oplossingen
Redoxreacties begrijpen
* Oxidatie: Verlies van elektronen
* Reductie: Winst van elektronen
* Redoxreactie: Een reactie waarbij zowel oxidatie als reductie betrokken zijn.
Activiteitenreeks
De reactiviteit van metalen wordt samengevat in de activiteitenreeks. Metalen hoger in de reeks hebben een grotere kans elektronen te verliezen (oxideren) en metalen lager in de reeks te verdringen.
* Meer actieve metalen: Hoger in de activiteitenreeks.
* Minder actieve metalen: Lager in de activiteitenreeks.
De belangrijkste spelers
* Zilver (Ag): Minder actief dan koper.
* Koper (Cu): Actiever dan zilver.
De waarschijnlijke reactie
Omdat koper actiever is dan zilver, zal het worden geoxideerd (elektronen verliezen) en zilver verdringen uit een oplossing die zilverionen bevat:
Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
Uitleg:
* Koper (Cu) is geoxideerd: Het verliest twee elektronen en wordt een koper(II)-ion (Cu²⁺).
* Zilverionen (Ag⁺) worden gereduceerd: Ze krijgen elektronen en worden massief zilver (Ag).
Belangrijke opmerking: De specifieke ionen die in de oplossing aanwezig zijn, zullen bepalen of deze reactie daadwerkelijk mogelijk is. Als de oplossing bijvoorbeeld alleen koperionen bevat, zou de reactie niet plaatsvinden.
 Hoeveel atomen zijn er in de molecuul Agcl?
Hoeveel atomen zijn er in de molecuul Agcl?  Kunnen stoffen tegelijkertijd zuur en alkalisch zijn?
Kunnen stoffen tegelijkertijd zuur en alkalisch zijn?  Hoe scheid je de kleurstofcomponenten in een snoepcoating op M en ms?
Hoe scheid je de kleurstofcomponenten in een snoepcoating op M en ms?  Onderzoeksteam combineert twee katalysatoren om de gemeenschappelijke chemische productie veiliger en milieuvriendelijker te maken
Onderzoeksteam combineert twee katalysatoren om de gemeenschappelijke chemische productie veiliger en milieuvriendelijker te maken  Het principe dat verklaart dat materie niet wordt gecreëerd of vernietigd tijdens een chemische reactie?
Het principe dat verklaart dat materie niet wordt gecreëerd of vernietigd tijdens een chemische reactie?
 Wat zijn de structuren die insecten en andere bestuivers naar een bloem aantrekken?
Wat zijn de structuren die insecten en andere bestuivers naar een bloem aantrekken?  Wetenschappers ontwikkelen een raamwerk om de plasticuitstoot te meten en de inspanningen van de VN om de vervuiling terug te dringen te versterken
Wetenschappers ontwikkelen een raamwerk om de plasticuitstoot te meten en de inspanningen van de VN om de vervuiling terug te dringen te versterken  Nieuw algoritme combineert kwaliteit en kwantiteit in satellietbeelden
Nieuw algoritme combineert kwaliteit en kwantiteit in satellietbeelden Amerikaanse milieugroeperingen klagen over terugdraaien van natuurbescherming
Amerikaanse milieugroeperingen klagen over terugdraaien van natuurbescherming Waarom de wetenschap over risicobeperking wordt betwist?
Waarom de wetenschap over risicobeperking wordt betwist?
Hoofdlijnen
- Wat hebben dominante en recessieve allelen gemeen?
- Is een wortel haarcelplant of een dierencel?
- Beschrijf de make -up van kern?
- Wat zijn twee organellen die samenwerken in de cel?
- Wat is de rol van fotosynthese in de voedselketen?
- Datawetenschap onthult universele regels voor het vormgeven van cellen in elektriciteitscentrales
- Wat is homeostaris?
- Wat zijn de drie belangrijkste factoren die aquatische ecosystemen regeren?
- Wie was de eerste die de ontwikkelde cultuurplaatmethode pathogenen identificeerde?
- Onderzoekers maken een fotografische film van een moleculaire schakelaar
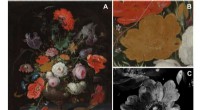
- Chemische en optische beeldvorming verklaren waarom een roos zijn kleur verloor op een beroemd schilderij
- Een manier ontwerpen om zuurstof injecteerbaar te maken

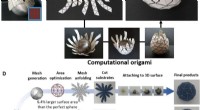
- Computationele origami:een universele methode om 3D-gebogen oppervlakken te omwikkelen met niet-rekbare materialen
- Chemie digitaliseren met een slimme roerstaaf

 Wat voor soort energietransformatie treedt op als de waterkrachtcentrales worden omgezet?
Wat voor soort energietransformatie treedt op als de waterkrachtcentrales worden omgezet?  Wat is transcriptie en wat zijn de belangrijkste stappen in dit proces?
Wat is transcriptie en wat zijn de belangrijkste stappen in dit proces?  Wordt sedimentaire rots na miljoenen jaren metamorf metamorf?
Wordt sedimentaire rots na miljoenen jaren metamorf metamorf?  De diepste en meest actieve huidverdeling wordt de?
De diepste en meest actieve huidverdeling wordt de?  Wat zijn feiten over granieten rock?
Wat zijn feiten over granieten rock?  Herscheppen van het geluid van het islamitische verleden van de moskee van Cordoba
Herscheppen van het geluid van het islamitische verleden van de moskee van Cordoba Onderzoekers melden nieuwe varensoorten uit Yunnan, China
Onderzoekers melden nieuwe varensoorten uit Yunnan, China  Hoe beïnvloedt windenergie de aarde?
Hoe beïnvloedt windenergie de aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

