
Wetenschap
Oplossen van ammoniak in water:inzicht in de NH3 + H2O-reactie
Hier is een nauwkeurigere weergave:
NH3 (water) + H2O (l) ⇌ NH4+ (water) + OH- (water)
Uitleg:
* NH3 (aq) :Ammoniak opgelost in water, waardoor een waterige oplossing ontstaat.
* H2O(l) :Vloeibaar water.
* NH4+ (water) :Ammoniumion, een positief geladen ion dat wordt gevormd wanneer ammoniak een proton (H+) uit water accepteert.
* OH- (aq) :Hydroxide-ion, een negatief geladen ion dat wordt gevormd wanneer water een proton verliest.
* ⇌ :De dubbele pijl geeft aan dat de reactie omkeerbaar is. Het kan in beide richtingen plaatsvinden, wat betekent dat ammonium- en hydroxide-ionen kunnen reageren om ammoniak en water te vormen.
Belangrijkste punten:
* Evenwicht: De reactie bereikt een evenwichtstoestand waarin de snelheden van de voorwaartse en achterwaartse reacties gelijk zijn.
* Basisoplossing: De aanwezigheid van hydroxide-ionen (OH-) maakt de oplossing basisch.
* Zwakke basis: Ammoniak is een zwakke base omdat het in water slechts gedeeltelijk ioniseert, wat betekent dat het niet al zijn elektronen afstaat om hydroxide-ionen te vormen.
Deze reactie is belangrijk omdat deze de fundamentele aard van ammoniak aantoont en het vermogen ervan om protonen in water te accepteren. Het is ook relevant voor het begrijpen van de pH van oplossingen die ammoniak bevatten.
 Hoe technologische vooruitgang het milieu vormgeeft:risico's, gebruik van hulpbronnen en verwijdering
Hoe technologische vooruitgang het milieu vormgeeft:risico's, gebruik van hulpbronnen en verwijdering  Welke van deze elementen zijn geen diatomic kaliumchloorjodium of waterstof?
Welke van deze elementen zijn geen diatomic kaliumchloorjodium of waterstof?  Onderzoekers bestuderen historische ontwikkelingen van het periodiek systeem van chemische elementen
Onderzoekers bestuderen historische ontwikkelingen van het periodiek systeem van chemische elementen Wat is het anion van bariumjodide?
Wat is het anion van bariumjodide?  Hybride orbitalen die worden gebruikt door chloor in CLF5?
Hybride orbitalen die worden gebruikt door chloor in CLF5?
 5 kritieke tekenen dat de bliksem op het punt staat in te slaan
5 kritieke tekenen dat de bliksem op het punt staat in te slaan  Fettuccine Rock zou het leven op Mars kunnen signaleren
Fettuccine Rock zou het leven op Mars kunnen signaleren  Welke keuzes worden gedefinieerd als de primaire lens waardoor leden van een cultuur worden geobserveerd en sense wereld is?
Welke keuzes worden gedefinieerd als de primaire lens waardoor leden van een cultuur worden geobserveerd en sense wereld is?  Moss tapijten helpen erosie te stoppen
Moss tapijten helpen erosie te stoppen Klimaatmodellen kunnen decadale regenvalvariaties op het Tibetaanse plateau voorspellen
Klimaatmodellen kunnen decadale regenvalvariaties op het Tibetaanse plateau voorspellen
Hoofdlijnen
- Wat is een Alektropia?
- Waarom kunnen we levende cellen niet zien met behulp van een elektronenmicroscoop?
- Wat is signaalhypothese?
- Wat is de ademhaling van Paramecium?
- Welke enzymen bouwen DNA?
- Natuurlijke selectie begrijpen:de kernprincipes van evolutie
- Nu waren gestrest? Geschiedenis toont de oudste emotie
- Is Tendril van een plant en phylloclade opuntia homoloog of analoog?
- Wat doet een biofysicus?
- Wat zeekomkommers ons kunnen leren over zelfverdediging

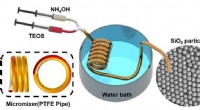
- Wetenschappers gebruiken een teflonpijp om een goedkope, eenvoudige reactor voor de synthese van silicadeeltjes
- Nieuwe draaitafelachtige katalytische reactor belooft duurzamere chemische productie

- Het begrijpen van bederf- en kwaliteitsproblemen kan de Amerikaanse ambachtelijke kaasindustrie verbeteren

- Wetenschappers vinden milieuvriendelijke manier om spijkerbroeken te verven

 Waarom is geothermische energie zo populair?
Waarom is geothermische energie zo populair?  Onderzoekers vinden nieuwe vorm voor hydrofobe moleculen in water
Onderzoekers vinden nieuwe vorm voor hydrofobe moleculen in water Fluorescentie-activerend bèta-vat-eiwit voor het eerst helemaal opnieuw gemaakt
Fluorescentie-activerend bèta-vat-eiwit voor het eerst helemaal opnieuw gemaakt Wetenschappers onthullen hoe verminderd zee-ijs in de Barentsz-Kara-zeeën de sneeuwbedekking in Eurazië kan vergroten
Wetenschappers onthullen hoe verminderd zee-ijs in de Barentsz-Kara-zeeën de sneeuwbedekking in Eurazië kan vergroten  Wetenschappers schatten de levensduur van wolharige mammoeten op 60 jaar met behulp van DNA-methylatie
Wetenschappers schatten de levensduur van wolharige mammoeten op 60 jaar met behulp van DNA-methylatie  Wanneer de maan vol is of dichter bij de zon is?
Wanneer de maan vol is of dichter bij de zon is?  Op welke twee manieren kunnen cellen energie verkrijgen als er geen zuurstof aanwezig is?
Op welke twee manieren kunnen cellen energie verkrijgen als er geen zuurstof aanwezig is?  Waarom zijn wetenschappers in staat om rotsen te gebruiken, ontdekken dat een vulkaan explosief of niet -explosief is?
Waarom zijn wetenschappers in staat om rotsen te gebruiken, ontdekken dat een vulkaan explosief of niet -explosief is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

