
Wetenschap
IJzer- en kaliumthiocyanaat:de bloedrode reactie begrijpen
Het metaalelement dat oplost in een salpeterzuuroplossing en bloedrood kleurt bij een kaliumthiocyanaattest is ijzer (Fe) .
Dit is waarom:
* Oplossen in salpeterzuur: IJzer reageert met salpeterzuur en vormt ijzer(III)-ionen (Fe³⁺) in oplossing.
* Kaliumthiocyanaattest: Wanneer kaliumthiocyanaat (KSCN) wordt toegevoegd aan een oplossing die ijzer(III)-ionen bevat, vormt het een bloedrood gekleurd complexion, [Fe(SCN)]²⁺. Dit complexe ion is verantwoordelijk voor de karakteristieke bloedrode kleur.
De reactie kan als volgt worden samengevat:
Fe(s) + 4 HNO₃(aq) → Fe(NO₃)₃(aq) + NO(g) + 2 H₂O(l)
Fe³⁺(aq) + SCN⁻(aq) → [Fe(SCN)]²⁺(aq)
 Wat is de enthalpie van water bij kamertemperatuur?
Wat is de enthalpie van water bij kamertemperatuur?  Waterstofauto's voor de massa een stap dichter bij de realiteit, dankzij UCLA-uitvinding
Waterstofauto's voor de massa een stap dichter bij de realiteit, dankzij UCLA-uitvinding Waarom wordt zout in heuvelachtige gebieden gebruikt om ijs te verwijderen, maar aan de andere kant zou het fabriek zijn om ijs te maken?
Waarom wordt zout in heuvelachtige gebieden gebruikt om ijs te verwijderen, maar aan de andere kant zou het fabriek zijn om ijs te maken?  Welke van de grote gassen bevat warmte?
Welke van de grote gassen bevat warmte?  Welke massa CCL4 wordt gevormd door de reactie van 8,00 g methaan met een overtollig chloride?
Welke massa CCL4 wordt gevormd door de reactie van 8,00 g methaan met een overtollig chloride?
Hoofdlijnen
- Wat zijn endorfines?
- Waaruit RNA samengesteld?
- Hoe vervuiling de genetica van dieren verandert:impact op diversiteit, mutaties en gezondheid van ecosystemen
- De giftige suikerboom:de evolutionaire geschiedenis van een kankerachtig suikergen in kaart brengen
- Waar ontwikkelt het embryo zich bij mensen?
- Studie onderzoekt conflict tussen boeren en roofdieren
- Wat is een externe bedekking die alle plantencellen hebben en niet in dierlijke cellen gevonden?
- Wat is een natuurlijke organisatie?
- Wiens systeem van klasse en het benoemen van organismen is vandaag nog steeds in gebruik?
- Autoplastics omzetten in schuim met kokosolie

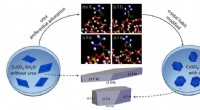
- Het effect van ureumadditieven op de fysisch-chemische eigenschappen van kristallen
- Autonome zelfgenezing gezien in piëzo-elektrische moleculaire kristallen

- Hoe u de hoogte van een ruit kunt berekenen:stapsgewijze handleiding

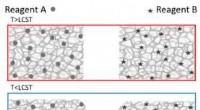
- Studie initieert chemische reacties door materialen te koelen in plaats van ze te verwarmen
 Wat gebeurt er met de luidheid van een geluid als oppervlakte -trillende lichaam wordt verminderd?
Wat gebeurt er met de luidheid van een geluid als oppervlakte -trillende lichaam wordt verminderd?  Voorkomen mensen dat vliegen afluisteren?
Voorkomen mensen dat vliegen afluisteren?  Wetenschappers laten zien dat er niets saai is aan het zien drogen van verf
Wetenschappers laten zien dat er niets saai is aan het zien drogen van verf  Is een Golf Tee -isolator of dirigent?
Is een Golf Tee -isolator of dirigent?  Bewegingsmagnetisme en een geleider zullen wat creëren?
Bewegingsmagnetisme en een geleider zullen wat creëren?  Endocriene klieren zijn afgeleid van welk type weefsel?
Endocriene klieren zijn afgeleid van welk type weefsel?  Een Europese studie onderzoekt hoe de landbouw rivieren beïnvloedt
Een Europese studie onderzoekt hoe de landbouw rivieren beïnvloedt  Nieuwe ontdekking opent nieuwe weg voor productie met hoge titer van drop-in biobrandstoffen
Nieuwe ontdekking opent nieuwe weg voor productie met hoge titer van drop-in biobrandstoffen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

