
Wetenschap
Smeltpunten van ionische verbindingen:factoren en verklaringen
* Sterke elektrostatische krachten: Ionische verbindingen worden bij elkaar gehouden door sterke elektrostatische aantrekkingskrachten tussen tegengesteld geladen ionen. Deze krachten zijn erg sterk en vereisen een aanzienlijke hoeveelheid energie om te overwinnen.
* Kristalroosterstructuur: De ionen in ionische verbindingen vormen een zeer geordend, driedimensionaal kristalrooster. Deze opstelling maximaliseert de elektrostatische aantrekkingskracht tussen de ionen, waardoor de structuur zeer stabiel wordt.
* Hoge energie vereist voor het smelten: Om een ionische substantie te smelten, moet je voldoende energie leveren om de sterke elektrostatische bindingen te verbreken die de ionen bij elkaar houden. Hiervoor is veel warmte nodig, wat resulteert in hoge smeltpunten.
Voorbeelden:
* Natriumchloride (NaCl) heeft een smeltpunt van 801°C.
* Magnesiumoxide (MgO) heeft een smeltpunt van 2852°C.
Uitzonderingen:
Hoewel de meeste ionische verbindingen hoge smeltpunten hebben, zijn er enkele uitzonderingen:
* Verbindingen met grote ionen: Wanneer ionen erg groot zijn, zijn de elektrostatische krachten die ze bij elkaar houden zwakker. Dit kan resulteren in lagere smeltpunten.
* Verbindingen met een lage ladingsdichtheid: Als de ladingen op de ionen relatief klein zijn, zullen de elektrostatische krachten zwakker zijn, wat leidt tot lagere smeltpunten.
Over het geheel genomen is het veilig om te zeggen dat ionische stoffen over het algemeen bekend staan om hun hoge smeltpunten vanwege de sterke krachten die hun kristalroosters bij elkaar houden.
 Termietendarmmicroben kunnen de productie van biobrandstoffen ondersteunen
Termietendarmmicroben kunnen de productie van biobrandstoffen ondersteunen Wat gebeurt er als aluminium wordt toegevoegd aan water en koperchloride?
Wat gebeurt er als aluminium wordt toegevoegd aan water en koperchloride?  Inzicht in de oxidatietoestand van koolstof in glucose:een gedetailleerde uitleg
Inzicht in de oxidatietoestand van koolstof in glucose:een gedetailleerde uitleg  Aantal elektronen aanwezig in een neutraal bariumatoom?
Aantal elektronen aanwezig in een neutraal bariumatoom?  Wat is het grammolecuulgewicht van cabondioxide?
Wat is het grammolecuulgewicht van cabondioxide?
 FreshDirect-depot zorgt voor meer verkeer naar South Bronx
FreshDirect-depot zorgt voor meer verkeer naar South Bronx Onderzoekers verbinden microben in de schemerzone van de oceaan met de afbraak van taaie organische moleculen
Onderzoekers verbinden microben in de schemerzone van de oceaan met de afbraak van taaie organische moleculen Hoe zijn natuurlijke hulpbronnen nuttig voor ons?
Hoe zijn natuurlijke hulpbronnen nuttig voor ons?  Kunnen we voorspellen of een plantensoort exotisch zal worden?
Kunnen we voorspellen of een plantensoort exotisch zal worden?  Nieuwe studie geeft een cijfer over de zeespiegelstijging na het instorten van de Antarctische ijsplaten
Nieuwe studie geeft een cijfer over de zeespiegelstijging na het instorten van de Antarctische ijsplaten
Hoofdlijnen
- Onderzoekers tonen bewijs van 'geheugen' in cellen en moleculen
- Welke term verwijst naar de fasen die een organisme doorloopt vanaf de geboortedood?
- Wat is magakaryocyten?
- Wordt aangeboren immuniteit gevonden bij zoogdieren?
- Welke eiwitvezel wordt gebruikt voor cellulaire beweging en zijn extreem dun in grootte?
- Wat is de beste wetenschappelijke ontdekking?
- Wat zijn methanogenus?
- Hoe goed kennen mensen zichzelf eigenlijk?
- Wat geeft framework aan cel en helpt het te bewegen?
- Deze microben eten elektronen voor energie
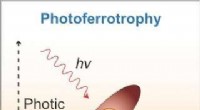
- Zijdevezels kunnen hightech natuurlijke metamaterialen zijn

- Wetenschappers verkrijgen met succes een synthetische groeifactor die compatibel is met het inheemse eiwit
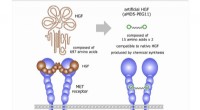
- Nieuwe technologie voor detectie van pathogenen aangedreven door lasers
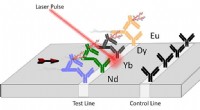
- Onderzoekers bewijzen dat water meerdere vloeibare toestanden heeft
 Ik zie geen ras en andere leugens om bestwil
Ik zie geen ras en andere leugens om bestwil Oplossen voor het bbp als u MPC en MPS
Oplossen voor het bbp als u MPC en MPS Wordt energie vrijgegeven of geabsorbeerd wanneer water van een vaste in vloeibaar gas verandert?
Wordt energie vrijgegeven of geabsorbeerd wanneer water van een vaste in vloeibaar gas verandert?  Hoe het volume CO2 te berekenen
Hoe het volume CO2 te berekenen  Wat zijn het soort mengsels?
Wat zijn het soort mengsels?  Wat zijn zwaveldioxide en stikstofoxiden?
Wat zijn zwaveldioxide en stikstofoxiden?  Wat is de massa van 15 mollen wolfraam?
Wat is de massa van 15 mollen wolfraam?  Hoe maak je Gak met Borax
Hoe maak je Gak met Borax
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

