
Wetenschap
Brønsted-Lowry-zuren en basen:definitie en belangrijkste kenmerken
* Zuren: Brønsted-Lowry-zuren zijn protondonoren . Ze doneren een proton (H+) aan een ander molecuul of ion.
* Basis: Brønsted-Lowry-basen zijn protonacceptoren . Ze accepteren een proton (H+) van een ander molecuul of ion.
Voorbeeld:
Bij de reactie van zoutzuur (HCl) met water (H2O):
* HCl (zuur) + H2O (base) → H3O+ (geconjugeerd zuur) + Cl- (geconjugeerde base)
* HCl staat een proton (H+) af om H3O+ (hydroniumion) te vormen, waardoor het een zuur wordt.
* H2O accepteert een proton (H+) om H3O+ te vormen, waardoor het een basis wordt.
Belangrijkste punten:
* De definitie van Brønsted-Lowry richt zich op de beweging van protonen tijdens chemische reacties.
* Deze definitie breidt de Arrhenius-definitie uit, die alleen zuren en basen in waterige oplossingen definieert.
* Het concept van geconjugeerde zuren en basen is essentieel in de Brønsted-Lowry-theorie.
 Is ammoniak amfoteer volgens het bronsted lawry-concept?
Is ammoniak amfoteer volgens het bronsted lawry-concept?  Waarom zijn er voor en na de reactie hetzelfde aantal deeltjes?
Waarom zijn er voor en na de reactie hetzelfde aantal deeltjes?  Wat wordt er tijdens één enkele draai van de citroenzuurcyclus gegenereerd?
Wat wordt er tijdens één enkele draai van de citroenzuurcyclus gegenereerd?  Wordt warmte beter uitgevoerd naarmate de moleculen verder uit elkaar in een stof zijn?
Wordt warmte beter uitgevoerd naarmate de moleculen verder uit elkaar in een stof zijn?  Nieuwe inzichten in een oud medicijn:wetenschappers ontdekken waarom aspirine zo goed werkt
Nieuwe inzichten in een oud medicijn:wetenschappers ontdekken waarom aspirine zo goed werkt
 Plotselinge overstromingen in Jordanië:sirenes en evacuatieplannen zijn geen vervanging voor onderwijs en communicatie
Plotselinge overstromingen in Jordanië:sirenes en evacuatieplannen zijn geen vervanging voor onderwijs en communicatie Ruimtegebaseerde lidar werpt nieuw licht op plankton
Ruimtegebaseerde lidar werpt nieuw licht op plankton Wetenschappers beginnen de diepten van de Indische Oceaan op de Seychellen te verkennen
Wetenschappers beginnen de diepten van de Indische Oceaan op de Seychellen te verkennen Hoe lokale gemeenschappen afhankelijk zijn van de ivoren palmboom aan de kust van Ecuador
Hoe lokale gemeenschappen afhankelijk zijn van de ivoren palmboom aan de kust van Ecuador  Tweederde van het land op aarde is op tempo om water te verliezen naarmate het klimaat warmer wordt
Tweederde van het land op aarde is op tempo om water te verliezen naarmate het klimaat warmer wordt
Hoofdlijnen
- Werken onze visserijwetten? Vraag maar naar gag grouper
- Wat maakt een uitleg goed genoeg?
- Wat is gebouwd als aminozuren aansluiten?
- Reproductieve cellen gaan door welk proces?
- Wat is uitbreiding in wetenschappelijke termen?
- Hoe vind je genen op de chromosomen van mensen?
- Professionele gids voor het isoleren van mRNA uit cellen
- Welk stuk van het apparaat zou worden gebruikt om aan te tonen dat een weefsel van hetzelfde type cellen bevat?
- Dierenartsen waarschuwen dat antivries giftig is voor huisdieren en mensen
- Forensisch chemicus stelt zweetteststrip voor als vervanging voor ademanalyse

- Video:Hortensia's, de vreemde van kleur veranderende bloemen

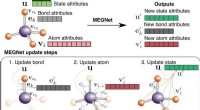
- Ingenieurs gebruiken grafieknetwerken om eigenschappen van moleculen en kristallen nauwkeurig te voorspellen
- Neutronen optimaliseren hoogrendementskatalysator voor groenere benadering van biobrandstofsynthese
- Chemici maken nieuw quasikristalmateriaal van bouwstenen voor nanodeeltjes

 Hoe mijnbouwbedrijven werknemers beter kunnen beschermen tegen letsel en overlijden
Hoe mijnbouwbedrijven werknemers beter kunnen beschermen tegen letsel en overlijden Computersimulaties verdiepen ons begrip van hoe medicijnen in het bloed terechtkomen
Computersimulaties verdiepen ons begrip van hoe medicijnen in het bloed terechtkomen  Wat is een kloof in de geografie?
Wat is een kloof in de geografie?  Aan welke rotsen kunnen graniet zich inleveren?
Aan welke rotsen kunnen graniet zich inleveren?  Noem twee veel voorkomende energieconversies met elektrische energie?
Noem twee veel voorkomende energieconversies met elektrische energie?  Maleisië laat het regenen terwijl Indonesische smog de lucht vervuilt
Maleisië laat het regenen terwijl Indonesische smog de lucht vervuilt Hoe maak je een model menselijke huidcel?
Hoe maak je een model menselijke huidcel?  Welke chemische stof is Hoci?
Welke chemische stof is Hoci?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

