
Wetenschap
Ammoniak als basis:de Brønsted-Lowry-definitie begrijpen
Hier is hoe het werkt:
* Brønsted-Lowry-definitie: Deze definitie definieert een zuur als protondonor en een base als protonacceptor.
* Ammoniakreactie: Wanneer ammoniak reageert met water, accepteert het een proton uit een watermolecuul en vormt het ammoniumion (NH₄⁺) en hydroxide-ion (OH⁻):
```
NH₃(aq) + H₂O(l) ⇌ NH₄⁺(aq) + OH⁻(aq)
```
* Protonacceptatie: Omdat ammoniak bij deze reactie een proton (H⁺) krijgt, fungeert het als een base.
Belangrijkste punten:
* Dankzij het enige elektronenpaar op het stikstofatoom kan ammoniak gemakkelijk een proton accepteren.
* Ook de vorming van hydroxide-ionen (OH⁻) bij de reactie is kenmerkend voor een base.
Daarom wordt ammoniak, op basis van zijn vermogen om een proton te accepteren, geclassificeerd als een base volgens de Brønsted-Lowry-definitie.
 Hoe boomsoorten schimmelpartners verbinden in een grootschalig bosecosysteem
Hoe boomsoorten schimmelpartners verbinden in een grootschalig bosecosysteem  Wat is een plotselinge droogte? Een aardwetenschapper legt het uit
Wat is een plotselinge droogte? Een aardwetenschapper legt het uit  Vanuatu-bedreiging voor vulkaanuitbarsting neemt af:wetenschappers
Vanuatu-bedreiging voor vulkaanuitbarsting neemt af:wetenschappers ASA's Aqua-satelliet vindt een extra-tropische cycloon Cimaron
ASA's Aqua-satelliet vindt een extra-tropische cycloon Cimaron Factoren die van invloed zijn op de ademhaling in planten
Factoren die van invloed zijn op de ademhaling in planten
Hoofdlijnen
- Het vermogen van een organisme om schommelingen in biotische en abiotische omgevingsfactoren te weerstaan?
- Welk bioom is het meest stabiel en de grootste?
- Onderzoekers voltooien eerste uitgebreide dreigingsanalyse van alle bomen in de VS
- Welke klier laat zijn secretie in de bloedbaan vrij?
- Wat zijn halfgeleiders?
- Is schimmel een levend of niet -leven?
- Wat is het proces door welke organismen met gewenste eigenschappen eerder overleven?
- Waarom verspreidt voedselkleuring zich in water?
- Wat voor soort micro-organisme kan ons ziek maken?
- Neutronentomografie:inzicht in het inwendige van tanden, wortel ballen, batterijen, en brandstofcellen

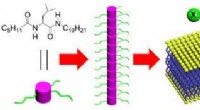
- Een nieuwe methode om ionen door celmembranen te transporteren op basis van een enkel aminozuur
- Gehyperpolariseerde proton-MRI gebruikt om metabolische processen in realtime te observeren

- Video:Hoeveel weegt een wolk?

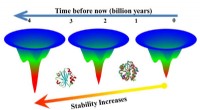
- Eiwitten die tegen de hitte kunnen
 Door de mens gemaakte eilanden komen vaker voor dan je denkt
Door de mens gemaakte eilanden komen vaker voor dan je denkt  Wat is het omliggende membraan dat bestaat uit 8 kernen in een bloeiende vrouwelijke gametophyt?
Wat is het omliggende membraan dat bestaat uit 8 kernen in een bloeiende vrouwelijke gametophyt?  Vooruitgang op weg naar een biologische brandstofcel?
Vooruitgang op weg naar een biologische brandstofcel?  Ontsteekt een zwart gat het koude hart van de Phoenix?
Ontsteekt een zwart gat het koude hart van de Phoenix?  Wat zijn de manieren waarop problemen van optische telescopen hebben gewerkt?
Wat zijn de manieren waarop problemen van optische telescopen hebben gewerkt?  Onderzoekers ontwikkelen nieuw superkritisch wateroxidatiesysteem
Onderzoekers ontwikkelen nieuw superkritisch wateroxidatiesysteem Waarom is het op dit moment in 2022 niet donker buiten?
Waarom is het op dit moment in 2022 niet donker buiten?  Wat betekent het woord esthetiek?
Wat betekent het woord esthetiek?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

