
Wetenschap
Stikstof- en zuurstofverhouding:impact op de eigenschappen van verbindingen
1. Verschillende chemische formules:
* Stikstofmonoxide (NO): Eén stikstofatoom en één zuurstofatoom.
* Stikstofdioxide (NO₂): Eén stikstofatoom en twee zuurstofatomen.
* Lachgas (N₂O): Twee stikstofatomen en één zuurstofatoom.
* Stikstoftrioxide (N₂O₃): Twee stikstofatomen en drie zuurstofatomen.
* Stikstofpentoxide (N₂O₅): Twee stikstofatomen en vijf zuurstofatomen.
Elk van deze verbindingen heeft een aparte chemische formule, die de specifieke verhouding van stikstof- en zuurstofatomen weerspiegelt.
2. Chemische eigenschappen:
* Reactiviteit: Verschillende verbindingen vertonen verschillende reactiviteit. NO is bijvoorbeeld een zeer reactief gas, terwijl N2O relatief niet-reactief is.
* Oxidatietoestanden: De variërende verhoudingen van stikstof en zuurstof leiden tot veranderingen in de oxidatietoestand van stikstof. Dit beïnvloedt hun rol in chemische reacties, of ze nu als oxidatie- of reductiemiddel werken.
* Verbinding: De verschillende verhoudingen beïnvloeden de soorten gevormde bindingen (enkel, dubbel, drievoudig) en hun sterkte.
3. Fysieke eigenschappen:
* Staat van de materie: Bij kamertemperatuur zijn sommige stikstofoxiden gassen (NO, NO₂, N₂O), terwijl andere vaste stoffen zijn (N₂O₅).
* Kleur: Verschillende verbindingen kunnen verschillende kleuren hebben. NO₂ is bijvoorbeeld een roodbruin gas, terwijl NO kleurloos is.
* Kookpunt en smeltpunt: De verhoudingen beïnvloeden de sterkte van de intermoleculaire krachten, waardoor de kook- en smeltpunten worden beïnvloed.
4. Biologische effecten:
* Toxiciteit: Sommige stikstofoxiden zijn zeer giftig, zoals NO₂, wat ademhalingsproblemen kan veroorzaken. Anderen, zoals N₂O, hebben verdovende eigenschappen.
Voorbeelden:
* Stikstofmonoxide (NO): Werkt als een signaalmolecuul in het lichaam en is betrokken bij de verwijding van bloedvaten.
* Stikstofdioxide (NO₂): Een belangrijke luchtverontreinigende stof, die bijdraagt aan smog en ademhalingsproblemen.
* Lachgas (N₂O): Een broeikasgas en verdovingsmiddel dat in de tandheelkunde wordt gebruikt.
Samengevat: De verhouding tussen stikstof- en zuurstofatomen is een cruciale factor die de chemische formule, fysische eigenschappen, reactiviteit en biologische effecten van een verbinding bepaalt. Elke combinatie van stikstof en zuurstof creëert een aparte verbinding met unieke eigenschappen.
Hoofdlijnen
- Welke structuur is in een plantencel maar geen bacteriële of dierlijke cel?
- Volgens de celtheorie voeren welke structuren basisfuncties van levende wezens uit?
- Wat is een uniceller organisme?
- Wat zijn de aanpassingen van een Jarrah -boom?
- Hoe een organisme eruit ziet, ongeacht de allelen van het type wordt gerefereerd als wat?
- Operanen:genclusters en regulatie begrijpen
- Welke structurele rol spelen fosfolipiden in cellen?
- Wat zijn de 60 wetenschapstakken?
- Wetenschappers ontwikkelen nieuwe techniek om het verborgen genoom te onthullen
- Onderzoekers ontdekken een nieuw anorganisch materiaal met de laagste thermische geleidbaarheid ooit gerapporteerd

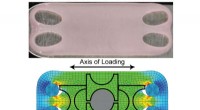
- Kunstkraakbeen onder spanning zo sterk als natuurlijk materiaal
- Fotochemische deracemisatie van chirale verbindingen bereikt

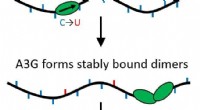
- Een als door te bewerken, twee als door wegversperring:menselijk eiwit bestrijdt HIV als monomeer en dimeer
- NIST pH-standaardreferentiematerialen ondersteunen een van de meest gemeten eigenschappen van de productie

 Hoe is het triest een voorbeeld van de relatie tussen biotische en abiotische delen ecosysteem?
Hoe is het triest een voorbeeld van de relatie tussen biotische en abiotische delen ecosysteem?  Wanneer formuleerde Robert Hooke de wet van elasticiteit?
Wanneer formuleerde Robert Hooke de wet van elasticiteit?  Als het aantal elektronen en protonen niet hetzelfde is, hoe noem je dit dan?
Als het aantal elektronen en protonen niet hetzelfde is, hoe noem je dit dan?  Betekent hogere of lagere frequentie meer energie?
Betekent hogere of lagere frequentie meer energie?  Wie bedacht het systeem van plantenclassificatie?
Wie bedacht het systeem van plantenclassificatie?  Is het waar dat Albert Einstein rijdt?
Is het waar dat Albert Einstein rijdt?  Welke verbinding wordt gebruikt voor het coaten van tapes met tape -recorder?
Welke verbinding wordt gebruikt voor het coaten van tapes met tape -recorder?  Supercomputers kunnen cyberdreigingen opsporen
Supercomputers kunnen cyberdreigingen opsporen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


