
Wetenschap
Moleculaire dipoolmomenten:wanneer verdwijnen ze?
Hier is een overzicht:
* Bonddipolen: Wanneer twee atomen met verschillende elektronegativiteit een covalente binding vormen, worden de elektronen ongelijk verdeeld. Dit resulteert in een gedeeltelijke positieve lading op het minder elektronegatieve atoom en een gedeeltelijke negatieve lading op het meer elektronegatieve atoom, waardoor een dipoolbinding ontstaat.
* Moleculair dipoolmoment: Het totale dipoolmoment van een molecuul is de vectorsom van al zijn bindingsdipolen. Als de bindingsdipolen elkaar opheffen, heeft het molecuul geen netto dipoolmoment en wordt het als niet-polair beschouwd. .
Voorbeeld:
* Kooldioxide (CO2):
* Elke C=O-binding heeft een sterke dipool, waarbij het zuurstofatoom meer elektronegatief is.
* De twee C=O-bindingen zijn lineair georiënteerd en wijzen in tegengestelde richtingen.
*De bindingsdipolen heffen elkaar op, waardoor het CO2-molecuul niet-polair wordt.
Belangrijk punt: De vorm van het molecuul en de rangschikking van de bindingsdipolen zijn cruciaal bij het bepalen van het totale dipoolmoment. Zelfs moleculen met sterke dipolen kunnen niet-polair zijn als hun geometrie leidt tot annulering van de dipolen.
 Een wetenschapper publiceert het resultaat van een experiment welke wetenschapsvaardigheden is dit?
Een wetenschapper publiceert het resultaat van een experiment welke wetenschapsvaardigheden is dit?  Wat is de roosterergie voor kaliumbromide?
Wat is de roosterergie voor kaliumbromide?  Welk element reageert met koolwaterstoffen tot Teflon en freon?
Welk element reageert met koolwaterstoffen tot Teflon en freon?  Hiërarchisch mesoporeuze titaniumdioxidematerialen voor energie- en milieutoepassingen
Hiërarchisch mesoporeuze titaniumdioxidematerialen voor energie- en milieutoepassingen Hoe kan de uitdrogingssynthese worden omgekeerd?
Hoe kan de uitdrogingssynthese worden omgekeerd?
 We maken neppoep in een laboratorium – om de sanitaire voorzieningen in Bangladesh te verbeteren
We maken neppoep in een laboratorium – om de sanitaire voorzieningen in Bangladesh te verbeteren Studie bevestigt gestreepte ijzerformaties afkomstig van geoxideerd ijzer
Studie bevestigt gestreepte ijzerformaties afkomstig van geoxideerd ijzer El Nino en het einde van de onderbreking van de opwarming van de aarde
El Nino en het einde van de onderbreking van de opwarming van de aarde Voorspelling van economische en demografische verschuivingen in de VS met een hogere resolutie
Voorspelling van economische en demografische verschuivingen in de VS met een hogere resolutie Voordelen en nadelen van natuurlijke omgevingen
Voordelen en nadelen van natuurlijke omgevingen
Hoofdlijnen
- Welk gevoel kan gemakkelijk worden gebruikt om de aanwezigheid van gist op kweekplaat te bepalen?
- Hoe is een plant stengel een voorbeeld van orgel?
- Hoe medicijnresistente ziekteverwekkerstammen elkaar ontmoeten en evolueren op bloembollen
- Hoe noem je een dier of bacteriën die zichzelf eet?
- What are the secretory cells of an ovarian follicle called?
- Hoe reproduceert milkweed?
- Zwaarste beenvissen ter wereld geïdentificeerd en correct benoemd
- Wat zijn de vijf kenmerken van een levend wezen?
- Wat is de moleculaire structuur van adenine?
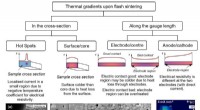
- Solid-state batterijen kunnen schoner worden gemaakt door flash-sintering op te schalen
- Optimalisatie van organische laagextractie met natriumcarbonaat

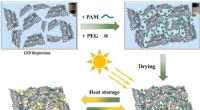
- Onderzoekers stellen een eenstapsstrategie voor om op grafeen gebaseerde composietfaseveranderingsmaterialen te synthetiseren
- Nul tot held:over het hoofd gezien materiaal kan onze ecologische voetafdruk helpen verkleinen

- Verbetering van de levensduur van bio-elektroden voor omzetting van zonne-energie

 Waar wordt bodemerosie gevonden?
Waar wordt bodemerosie gevonden?  Welke van de volgende zijn chemische eigenschappen:veranderingen in temperatuur, rijping, verdamping, vochtigheid?
Welke van de volgende zijn chemische eigenschappen:veranderingen in temperatuur, rijping, verdamping, vochtigheid?  Seizoensgids voor sterrenbeelden op het noordelijk halfrond
Seizoensgids voor sterrenbeelden op het noordelijk halfrond  Wat voor soort energie is een stuk radioactieve Metla?
Wat voor soort energie is een stuk radioactieve Metla?  Welke maan is het enige grote in zonnestelsel met een retrograde baan?
Welke maan is het enige grote in zonnestelsel met een retrograde baan?  Wetenschappers doorgronden diepe ventilatie in de Stille Oceaan
Wetenschappers doorgronden diepe ventilatie in de Stille Oceaan Amerikaanse brandweerlieden bestrijden zelfmoordgedachten na de brand
Amerikaanse brandweerlieden bestrijden zelfmoordgedachten na de brand DNA bestaat uit wat?
DNA bestaat uit wat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

