
Wetenschap
Stikstofchloride (NCl₃):de polariteit ervan begrijpen
* Moleculaire geometrie: NCl₃ heeft een trigonale piramidevorm. Het stikstofatoom bevindt zich in het midden, met drie chlooratomen eraan vast en een eenzaam elektronenpaar op de stikstof.
* Verschil in elektronegativiteit: Chloor is elektronegatiever dan stikstof. Dit betekent dat de chlooratomen de gedeelde elektronen in de N-Cl-bindingen dichter naar zich toe trekken, waardoor gedeeltelijke negatieve ladingen (δ-) op de chlooratomen en een gedeeltelijke positieve lading (δ+) op het stikstofatoom ontstaan.
* Asymmetrische ladingsverdeling: De drie polaire N-Cl-bindingen en het eenzame paar op het stikstofatoom heffen elkaar niet op. Hierdoor ontstaat er een netto dipoolmoment in het molecuul, wijzend naar de chlooratomen.
Daarom is NCl₃, vanwege de polaire N-Cl-bindingen en de asymmetrische ladingsverdeling, een polair molecuul.
 Onderzoekers onderzoeken de veerkracht van de voedselvoorzieningsketen in de Stille Oceaan tijdens de COVID-19-pandemie
Onderzoekers onderzoeken de veerkracht van de voedselvoorzieningsketen in de Stille Oceaan tijdens de COVID-19-pandemie Onderzoekers nemen atmosferische effecten van Arctische sneeuwsmelt onder de loep
Onderzoekers nemen atmosferische effecten van Arctische sneeuwsmelt onder de loep Welke elementen worden vanzelf gevonden in de natuur?
Welke elementen worden vanzelf gevonden in de natuur?  De iconische Joshua Tree wordt met uitsterven bedreigd
De iconische Joshua Tree wordt met uitsterven bedreigd  De wijsheid van het kweken van parels
De wijsheid van het kweken van parels
Hoofdlijnen
- Wie zijn de beroemde bioloog en wat hun bijdragen?
- Kunnen bacteriecellen worden geclassificeerd als plantencellen?
- Wasberen lossen een eeuwenoude puzzel op, maar begrijpen ze die echt?
- Slapen spinnen? Uit onderzoek blijkt dat ze net als mensen kunnen dutten
- Wat bestaat uit cellulose en alleen gevonden in planten?
- Wat is het Perichondrium?
- Welke 4 organen zijn te vinden in planten?
- Hoe peulvruchten zuurstof geven aan symbiotische bacteriën in hun wortels
- Is het waar of onwaar dat mitose het proces is waarin kern van celverdeling?
- Kleverige koperionen dragen bij aan de vertraging van de katalysator

- De komende verstoring van OLED-technologieën

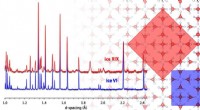
- Nieuwe kristallijne ijsvorm:wetenschappers verhelderen kristalstructuur voor exotisch ijs XIX
- Wetenschappers pionieren met het maken van programmeerbare kunstmatige weefsels van synthetische cellen

- Nieuwe methode om olie uit water te verwijderen

 Soorten spiegels en lenzen
Soorten spiegels en lenzen Op turf gebaseerde klimaatreconstructies komen in troebel water terecht?
Op turf gebaseerde klimaatreconstructies komen in troebel water terecht?  Wat zal geen stervorming veroorzaken?
Wat zal geen stervorming veroorzaken?  Waarom wordt koperoxide oxide genoemd?
Waarom wordt koperoxide oxide genoemd?  Wat leidde tot de ontdekking van verre pull -planeten?
Wat leidde tot de ontdekking van verre pull -planeten?  Wat zijn de reden dat wetenschappers moesten samenwerken, ontwikkelen de geologische kolom?
Wat zijn de reden dat wetenschappers moesten samenwerken, ontwikkelen de geologische kolom?  Hoe beïnvloeden bomen het weer?
Hoe beïnvloeden bomen het weer?  Hoeveel daglichturen in Mercurius?
Hoeveel daglichturen in Mercurius?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

