
Wetenschap
Kaliumnitraat oplossen in water:chemische vergelijking en uitleg
KNO₃(s) + H₂O(l) → K⁺(aq) + NO₃⁻(aq)
Dit is wat de vergelijking betekent:
* KNO₃(s) :Kaliumnitraat in vaste vorm.
* H₂O(l) :Water in vloeibare toestand.
* K⁺(aq) :Kaliumionen opgelost in water.
* NO₃⁻(aq) :Nitraationen opgelost in water.
Belangrijkste punten:
* De reactie is omkeerbaar , wat betekent dat de opgeloste ionen onder de juiste omstandigheden (zoals verdamping van het water) vast kaliumnitraat kunnen hervormen.
* De reactie is exotherm , wat betekent dat er warmte vrijkomt en de oplossing iets warmer wordt.
Opmerking: Het is belangrijk om te onthouden dat de vergelijking niet de daadwerkelijke chemische transformatie laat zien, maar alleen de verandering in de toestand en de gevormde ionen. De kaliumnitraatmoleculen reageren niet met water om nieuwe moleculen te vormen, ze dissociëren eenvoudigweg in ionen wanneer ze worden opgelost.
 Wat is chemisch gerelateerd aan glas?
Wat is chemisch gerelateerd aan glas?  Zal chloor reageren met natriumchloride?
Zal chloor reageren met natriumchloride?  Unieke ferro-elektrische microstructuur voor het eerst onthuld
Unieke ferro-elektrische microstructuur voor het eerst onthuld Gotcha! Wetenschappers nemen vingerafdrukken van eiwitten met behulp van hun trillingen
Gotcha! Wetenschappers nemen vingerafdrukken van eiwitten met behulp van hun trillingen Inzicht in de gasstroom voor verbeterde toepassingen voor schone energie
Inzicht in de gasstroom voor verbeterde toepassingen voor schone energie
 Duitsland zet waarschuwingssysteem in twijfel na dodelijke overstromingen
Duitsland zet waarschuwingssysteem in twijfel na dodelijke overstromingen Robots kunnen een revolutie teweegbrengen in de monitoring van het mariene milieu
Robots kunnen een revolutie teweegbrengen in de monitoring van het mariene milieu Wilt u uw gezondheid verbeteren? Ga naar een nationaal park en absorbeer de geluiden
Wilt u uw gezondheid verbeteren? Ga naar een nationaal park en absorbeer de geluiden  Wat voor soort leefomgeving leeft een cheeta?
Wat voor soort leefomgeving leeft een cheeta?  EPA stelt mijnbedrijf in staat vergunningen te verkrijgen in de buurt van de baai van Alaska
EPA stelt mijnbedrijf in staat vergunningen te verkrijgen in de buurt van de baai van Alaska
Hoofdlijnen
- Welke tak van de wetenschap doet botanicus?
- Wat is het voordeel van aseksuele reproductio?
- Plantencellen gebruiken welk molecuul om glucose te maken?
- Hoeveel genetische informatie wordt van ouder tot nakomelingen doorgegeven?
- De regel die beschrijft hoe een reeks nucleotiden?
- Dode walvis verrast zwemmers op iconisch strand van Rio
- Wat is Bioogical Science?
- Natuurbehoud werkt, en we worden er steeds beter in, zegt nieuw onderzoek
- DNA- en eiwitproductie:hoe uw genen uw lichaam vormen
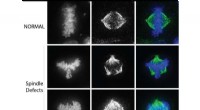
- Een nieuw mechanisme in celdeling ontdekken
- Gesimuleerd microzwaartekrachtsysteem gemaakt om te experimenteren met materialen

- Lasers en vlammen:techniek kan de prestaties van hightech materialen verfijnen

- Wetenschappers koken nieuwe recepten om zout uit zeewater te halen

- Nieuwe methode keert de zelfassemblage van vloeibare kristallen om

 Sucrose wordt verbrand om koolstofdioxide en water te produceren. wat is de evenwichtige vergelijking?
Sucrose wordt verbrand om koolstofdioxide en water te produceren. wat is de evenwichtige vergelijking?  Negen doden nadat Indonesische hoofdstad getroffen werd door nieuwjaarsoverstroming (Update)
Negen doden nadat Indonesische hoofdstad getroffen werd door nieuwjaarsoverstroming (Update) Nanogestructureerde filters gebruiken om vervuiling door scheepvaart te verminderen
Nanogestructureerde filters gebruiken om vervuiling door scheepvaart te verminderen Heeft AT-Rich of GC-rijk DNA een hogere smelttemperatuur?
Heeft AT-Rich of GC-rijk DNA een hogere smelttemperatuur?  Wat zijn de koninkrijken die meercellige organismen bevatten?
Wat zijn de koninkrijken die meercellige organismen bevatten?  Vetzuur: definitie, metabolisme en functie
Vetzuur: definitie, metabolisme en functie  Biodiversiteit:kunnen we waarde hechten aan de natuur?
Biodiversiteit:kunnen we waarde hechten aan de natuur? Hoe maakt de kern eiwit voor cel?
Hoe maakt de kern eiwit voor cel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

