
Wetenschap
Inzicht in de relatie tussen oxidatietoestand en zuurgraad
1. Elektronegativiteit en polariteit
* Hogere oxidatietoestand =positiever: Wanneer een element een hogere oxidatietoestand heeft, betekent dit dat het meer elektronen heeft verloren en positiever geladen is geworden.
* Grotere polarisatie: Deze positieve lading trekt elektronen sterker aan, wat leidt tot een meer gepolariseerde binding met het atoom waaraan het is bevestigd (meestal zuurstof in zure verbindingen).
* Gemakkelijkere protonendonatie: De gepolariseerde binding verzwakt de binding tussen het waterstofatoom en de zuurstof, waardoor het gemakkelijker wordt om de waterstof vrij te geven als een proton (H+), waardoor de zuurgraad toeneemt.
2. Inductief effect
* Elektronenopname: De positieve lading van de hogere oxidatietoestand kan de elektronendichtheid door het molecuul wegtrekken van het zuurstofatoom. Dit maakt de zuurstof meer elektronendeficiënt.
* Verbeterde zuurgraad: Het grotere elektronenzuigende vermogen van de zuurstof verzwakt de O-H-binding, waardoor het opnieuw gemakkelijker wordt om het proton te doneren en de zuurgraad te verhogen.
Voorbeelden
* Halogenen: Vergelijk HClO (hypochloorzuur) met HClO4 (perchloorzuur). Chloor in HClO4 heeft een hogere oxidatietoestand (+7) dan in HClO (+1), wat leidt tot een hogere zuurgraad.
* Zwaveloxiden: SO2 (zwaveldioxide) is een zwak zuur vergeleken met SO3 (zwaveltrioxide), dat een sterk zuur is. De hogere oxidatietoestand van zwavel in SO3 verhoogt de zuurgraad ervan.
* Carboxylzuren: De zuurgraad van carbonzuren neemt toe met elektronenzuigende groepen (bijvoorbeeld halogenen) die aan de koolstof naast de carboxylgroep zijn bevestigd. Deze groepen verhogen de oxidatietoestand van de koolstof, waardoor het carbonzuur zuurder wordt.
Belangrijke opmerking:
Hoewel deze trend voor veel gevallen geldt, zijn er uitzonderingen. De specifieke structuur van het molecuul en de aard van andere atomen in het molecuul kunnen ook de zuurgraad aanzienlijk beïnvloeden.
Laat het me weten als je specifiekere voorbeelden wilt of een bepaald molecuul wilt bespreken.
 Hoe heet het als een vaste stof voor kinderen in gas verandert?
Hoe heet het als een vaste stof voor kinderen in gas verandert?  Onderzoekers ontwikkelen een nieuwe manier om belangrijke biologische processen te bestuderen
Onderzoekers ontwikkelen een nieuwe manier om belangrijke biologische processen te bestuderen Wat is de exacte verhouding van natriumionen tot chloride in NaCl?
Wat is de exacte verhouding van natriumionen tot chloride in NaCl?  Wat hoort zwavelwater neon koolstof?
Wat hoort zwavelwater neon koolstof?  Eenvoudige en goedkope scheurgenezing van composieten op keramiekbasis
Eenvoudige en goedkope scheurgenezing van composieten op keramiekbasis
Hoofdlijnen
- De celtheorie vermeldt dat niet?
- Naam 3 Andere celorganellen die op een vergelijkbare manier uit membranensystemen bestaan als het membraan?
- Wat voor soort agriulturele planten bevatten eiwitten?
- De rol van Taq-polymerase in PCR
- Wat zijn de weefsels die combineren om een orgel te vormen?
- Bijtmiddelen in de microbiologie begrijpen:hoe ze vlekken aan cellen verankeren
- Welke structuren worden over het algemeen aangetroffen in prokaryotische cellen?
- Onderzoek verbetert multiplexmutagenese om de experimentele efficiëntie bij het bewerken van plantengenoom te vergroten
- Wat is het doel van een anjerkebloem?
- Wetenschappers programmeren eiwitten om precies te paren
- Etsproces verbetert de extractie van waterstof tijdens elektrolyse van water
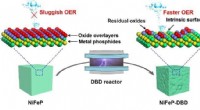
- Voor waterstofenergie, alledaagse materialen zijn misschien bijna net zo goed als prijzig platina

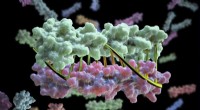
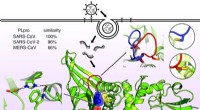
- Informatie over de moleculaire vorm van virussen die COVID-19 veroorzaken, SARS, en MERS onthult structurele overeenkomsten
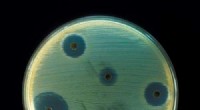
- Octapeptin:Vergeten antibioticum biedt hoop tegen de ergste superbacteriën
 Het beklimmen van de Mont Blanc een hele opgave terwijl Europa broeit
Het beklimmen van de Mont Blanc een hele opgave terwijl Europa broeit Waarom vertrouwen op nieuwe technologie de planeet niet zal redden?
Waarom vertrouwen op nieuwe technologie de planeet niet zal redden? Wat zijn de functies van enzym in het menselijk lichaam?
Wat zijn de functies van enzym in het menselijk lichaam?  Alle in Michigan bevestigde poema's waren mannelijk:waarom we geen vrouwtjes en kittens zien
Alle in Michigan bevestigde poema's waren mannelijk:waarom we geen vrouwtjes en kittens zien  Welk materiaal lijkt op piepschuim?
Welk materiaal lijkt op piepschuim?  De unieke onderzoeksprojecten
De unieke onderzoeksprojecten  Wat zijn twee voedingsstoffen die het GI -kanaal verlaten via het lymfestelsel?
Wat zijn twee voedingsstoffen die het GI -kanaal verlaten via het lymfestelsel?  UITLEG:Waarom South 's nachts meer dodelijke tornado's krijgt
UITLEG:Waarom South 's nachts meer dodelijke tornado's krijgt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

