
Wetenschap
Natrium in vloeibare ammoniak:reacties en eigenschappen uitgelegd
1. Ontbinding en ionisatie:
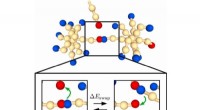
* Oplossing: Natriummetaal (Na) is gemakkelijk oplosbaar in vloeibare ammoniak (NH3). De ammoniakmoleculen, die polair zijn, omringen de natriumatomen en solvateren ze, waardoor het metaalrooster effectief wordt afgebroken.
* Ionisatie: Bij solvatatie verliezen natriumatomen hun buitenste elektron en vormen ze positief geladen natriumionen (Na+). De vrijgekomen elektronen worden opgelost door ammoniakmoleculen en vormen negatief geladen soorten die "geammoniseerde elektronen" (e-(NH3)x) worden genoemd.
2. Vorming van geammoniseerde elektronen:
* Elektronenvangst: De vrijgekomen elektronen zijn niet vrij, maar zitten gevangen in holtes gevormd door ammoniakmoleculen. Deze holtes creëren een "gesolvateerd elektron" met een karakteristieke blauwe kleur.
* Stabilisatie: De ammoniakmoleculen fungeren als een diëlektrisch medium, waardoor de elektrostatische aantrekkingskracht tussen de positieve en negatieve ionen wordt verlaagd en de gesolvateerde elektronen worden gestabiliseerd.
3. Oplossingseigenschappen:
* Kleur: De resulterende oplossing vertoont een diepblauwe kleur, die wordt toegeschreven aan de aanwezigheid van gesolvateerde elektronen.
* Geleidbaarheid: De oplossing wordt sterk elektrisch geleidend door de aanwezigheid van vrije ionen (Na+ en e-(NH3)x).
* Paramagnetisme: De gesolvateerde elektronen vertonen paramagnetisme, een eigenschap die geassocieerd wordt met ongepaarde elektronen.
4. Reacties en bijwerkingen:
* Reacties met protonen: De gesolvateerde elektronen zijn sterke reductiemiddelen en kunnen reageren met elke bron van protonen (H+). Dit kan leiden tot de vorming van waterstofgas (H2).
* Metaal-ammoniakcomplexen: Natriumionen kunnen ook complexen vormen met ammoniakmoleculen, wat verder bijdraagt aan de stabiliteit van de oplossing.
* Ontbinding: Na verloop van tijd kan de oplossing ontleden, vooral als er onzuiverheden aanwezig zijn. Deze ontleding kan leiden tot de vorming van natriumamide (NaNH2) en waterstofgas.
Samengevat:
Het oplossen van natrium in vloeibare ammoniak is een complex proces dat leidt tot een zeer reactieve, blauwe oplossing met unieke eigenschappen. Het is belangrijk op te merken dat deze reactie met zorg moet worden uitgevoerd, omdat er zeer reactieve materialen bij betrokken zijn en brandbare gassen kunnen ontstaan.
 Snelle emissiereducties zouden CO2-verwijdering en kosten onder controle houden
Snelle emissiereducties zouden CO2-verwijdering en kosten onder controle houden Spuitbussen van vervuiling, woestijnstormen, en bosbranden kunnen onweersbuien versterken
Spuitbussen van vervuiling, woestijnstormen, en bosbranden kunnen onweersbuien versterken Regenen, wegoverstromingen terwijl tropische storm Cristobal dichterbij komt
Regenen, wegoverstromingen terwijl tropische storm Cristobal dichterbij komt Studie onthult hoe de aardgasproductie in schalie kan worden verbeterd
Studie onthult hoe de aardgasproductie in schalie kan worden verbeterd Satellietogen Tropische storm Irma wervelt in oostelijke Atlantische Oceaan
Satellietogen Tropische storm Irma wervelt in oostelijke Atlantische Oceaan
Hoofdlijnen
- Hoeveel gemeenschappelijke namen een organisme ook heeft, heeft het er maar één?
- Leven gelukkige mensen langer?
- Begrijpen hoe pathogene schimmels hun koolhydraatpantser opbouwen
- De nacht zit vol met dieren, maar wetenschappers weten er heel weinig van
- Regelen lipiden de activiteit van genen?
- Osmose en diffusie:de verbinding begrijpen
- Wetenschappers ontwikkelen microben om herinneringen aan hun omgeving te vormen
- Welke van de volgende zou een bioloog niet studeren als hij of zij in veldcellulaire biologie werkte?
- Wat zijn vrije nucleotiden?
- E-nose ruikt mengsels van vluchtige organische stoffen

- Productie recyclebaar plastic stap dichterbij
- Doorbraak voor wetshandhavers om hennep en gecontroleerde marihuana snel te onderscheiden

- Kunstmatig synaptisch apparaat simuleert de functie van het menselijk brein
- Iowa's recordkoude temperaturen:een historisch overzicht

 Wat zijn kleine rotsendeeltjes weggegooid?
Wat zijn kleine rotsendeeltjes weggegooid?  Microplastics gevonden in oesters, mosselen aan de kust van Oregon, studie vondsten
Microplastics gevonden in oesters, mosselen aan de kust van Oregon, studie vondsten Wil ik een altijd-aan digitale assistent die altijd meeluistert?
Wil ik een altijd-aan digitale assistent die altijd meeluistert? Hoe voltooi je de dierenriempuzzelsleutel in aqworlds?
Hoe voltooi je de dierenriempuzzelsleutel in aqworlds?  Wat wordt bedoeld met germentatie?
Wat wordt bedoeld met germentatie?  De energieproducerende eenheden van een cel?
De energieproducerende eenheden van een cel?  Cruciaal voor het leven, oceanen krijgen kans in klimaatschijnwerpers
Cruciaal voor het leven, oceanen krijgen kans in klimaatschijnwerpers Waarom heb je de maan de laatste tijd gezien?
Waarom heb je de maan de laatste tijd gezien?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

