
Wetenschap
Atomen met twee ongepaarde elektronen:een uitgebreide gids
Inzicht in de elektronenconfiguratie
* Orbitalen: Elektronen bezetten specifieke energieniveaus die orbitalen worden genoemd. Elke orbitaal kan maximaal twee elektronen bevatten.
* Hunds regel: Bij het vullen van orbitalen binnen een subshell (zoals de p-subshell), zullen elektronen elke orbitaal afzonderlijk bezetten voordat ze paren vormen.
* Koppelen: Elektronen in dezelfde orbitaal zullen tegengestelde spins hebben.
Atomen vinden met twee ongepaarde elektronen
1. Identificeer het element: U moet het atoomnummer van het element weten om de elektronenconfiguratie te bepalen.
2. Schrijf de elektronenconfiguratie: Gebruik het periodiek systeem en het Aufbau-principe om de elektronenconfiguratie te schrijven. Koolstof (atoomnummer 6) heeft bijvoorbeeld de configuratie 1s² 2s² 2p².
3. Bekijk de p-subshell: De p-subshell heeft drie orbitalen (px, py, pz). Zoek naar elementen waarbij de p-subshell twee ongepaarde elektronen heeft.
Voorbeelden:
* Koolstof (C): 1s² 2s² 2p² - Twee ongepaarde elektronen in de 2p-orbitalen
* Zuurstof (O): 1s² 2s² 2p⁴ - Twee ongepaarde elektronen in de 2p-orbitalen
* Zwavel (S): 1s² 2s² 2p⁶ 3s² 3p⁴ - Twee ongepaarde elektronen in de 3p-orbitalen
Belangrijke opmerking: Dit is een vereenvoudigde uitleg. Het werkelijke aantal ongepaarde elektronen kan worden beïnvloed door factoren als hybridisatie en elektron-elektronenafstoting in complexere atomen.
 Wanneer een molecuul een elektron wint, is het wat geweest?
Wanneer een molecuul een elektron wint, is het wat geweest?  Versnelde ontdekkingssnelheid kan leiden tot effectievere hulpmiddelen om te stoppen met roken
Versnelde ontdekkingssnelheid kan leiden tot effectievere hulpmiddelen om te stoppen met roken Wat is de chemische formule voor vloeibare stikstof?
Wat is de chemische formule voor vloeibare stikstof?  Wat zou worden beschouwd als een organisch molecuul H20 NAC1 NaOH CH4?
Wat zou worden beschouwd als een organisch molecuul H20 NAC1 NaOH CH4?  Wat is een platina juf?
Wat is een platina juf?
Hoofdlijnen
- Internationale samenwerking werkt om schimmelresistent katoen te kweken
- Wat is de term voor structuur die geen nut heeft in een organisme?
- Een eiwitduo zorgt ervoor dat de chromosomen in de voortplantingscellen hun significante andere vinden
- Is een gespecialiseerde spiercelcel?
- Waarom zijn kalkoenen genetisch gemodificeerd?
- Waarom leveren fylogenetische bomen sterk bewijs van evolutie?
- Plantencellen:het enorme aantal planten begrijpen
- Biologische afvalwaterzuivering:voordelen, nadelen en beste praktijken
- Hersencellen:zijn neuronen levende organismen?
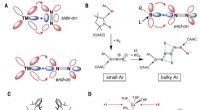
- Onderzoekers vinden verrassende bindingen van het overgangsmetaaltype tijdens het bouwen van nieuwe calcium(I)-complexen
- Het geheim van de beste seizoensgebonden warme chocolademelk? Het zit allemaal in de chemie!

- Inkjetprinten veelbelovend als nieuwe strategie voor het maken van e-textiel, studie vondsten

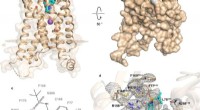
- Studie onthult structuur van receptor die betrokken is bij diabetes type 2 en meer
- Teamwerk in een molecuul

 Internationale SWOT-missie kan de voorspelling van overstromingen verbeteren
Internationale SWOT-missie kan de voorspelling van overstromingen verbeteren  Een man houdt een stalen bal van 4,0 kg in de hand, zijn arm is 70 cm lang en heeft massa van wat het magnitude -koppel om zijn schouder als hij recht maar 30 graden onder horizontaal is?
Een man houdt een stalen bal van 4,0 kg in de hand, zijn arm is 70 cm lang en heeft massa van wat het magnitude -koppel om zijn schouder als hij recht maar 30 graden onder horizontaal is?  Energie-efficiëntie:een aanwijzing voor politiek haalbaar klimaatbeleid
Energie-efficiëntie:een aanwijzing voor politiek haalbaar klimaatbeleid DNA is gecondenseerd in welke fasen?
DNA is gecondenseerd in welke fasen?  Hoe brengen koolhydraten zonne -energie over aan mensen?
Hoe brengen koolhydraten zonne -energie over aan mensen?  Wanneer een elektrisch fornuis -element heet genoeg is, geeft dit een saaie rode gloed af zover het niet langer gloeit wat er gebeurt?
Wanneer een elektrisch fornuis -element heet genoeg is, geeft dit een saaie rode gloed af zover het niet langer gloeit wat er gebeurt?  Onderzoeksvraag:Kunnen uw keukenbladen radioactief zijn?
Onderzoeksvraag:Kunnen uw keukenbladen radioactief zijn?  India geeft Volkswagen 24 uur om Dieselgate-boete te betalen
India geeft Volkswagen 24 uur om Dieselgate-boete te betalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

