
Wetenschap
Zuurstof versus xenon-ionisatie-energieën:een vergelijkende analyse
Dit is waarom:
* Elektronenconfiguratie: Zuurstof heeft de elektronenconfiguratie 1s²2s²2p⁴, terwijl xenon de configuratie [Kr]4d¹⁰5s²5p⁶ heeft. Dit betekent dat de buitenste elektronen in zuurstof zich in de 2p-subschaal bevinden, terwijl de buitenste elektronen in xenon zich in de 5p-subschaal bevinden.
* Afschermingseffect: De 5p-elektronen in xenon bevinden zich veel verder van de kern dan de 2p-elektronen in zuurstof. Ze ervaren een groter afschermend effect van de binnenste elektronen, waardoor de aantrekkingskracht tussen de kern en de buitenste elektronen wordt verminderd.
* Nucleaire lading: Xenon heeft een veel grotere nucleaire lading dan zuurstof, vanwege het grotere aantal protonen. Dit vergroot de aantrekkingskracht tussen de kern en zijn elektronen.
De grotere nucleaire lading in xenon is echter niet genoeg om het afschermende effect en de grotere afstand van de 5p-elektronen te overwinnen. Dit resulteert in een aanzienlijk lagere ionisatie-energie voor xenon vergeleken met zuurstof .
Samengevat:
* Zuurstof heeft een hogere ionisatie-energie dan xenon.
* Dit verschil is te wijten aan de combinatie van afschermende effecten, afstand tot de kern en nucleaire lading.
 19 EU-lidstaten registreren stikstofdioxideconcentraties boven de jaargrenswaarde in 2018
19 EU-lidstaten registreren stikstofdioxideconcentraties boven de jaargrenswaarde in 2018 Wat is het verschil tussen een natuurlijk en gecultiveerd bos?
Wat is het verschil tussen een natuurlijk en gecultiveerd bos?  Onderzoek naar outdoor- en beschermende kleding probeert fluorchemicaliën af te schudden
Onderzoek naar outdoor- en beschermende kleding probeert fluorchemicaliën af te schudden Koraaltransplantatie verhoogt de hoop op overleving van het Barrièrerif
Koraaltransplantatie verhoogt de hoop op overleving van het Barrièrerif In de harde hoek van Oeganda, herders vechten tegen klimaatverandering
In de harde hoek van Oeganda, herders vechten tegen klimaatverandering
Hoofdlijnen
- Wat zit er in het embryo?
- Hoe noem je een wetenschapper die weefsels studeert?
- Leg de betekenis van homeostase uit zoals toegepast op het levende organisme?
- Een enkel gen van de ene soort nemen en het naar de andere overbrengen is een voorbeeld van?
- Hoe is een cel levend wezen dat kern heeft geroepen?
- Welk element is het hoofd van het leven op basis van koolstoffamilies?
- Celdeling in planten:hoe celwanden worden samengesteld
- Wat zijn celgrenzen?
- In welk weefsel bevindt zich fagocyten?
- Deeltjes van alledaagse muurverven kunnen levende organismen schaden, maar een nieuw membraan vertoont hoge filtereffecten

- PowerPoint en LED-projector maken nieuwe techniek mogelijk voor zelfvouwende origami

- Wetenschappers identificeren elektronische en structurele dynamiek van katalytische centra in materialen met één Fe-atoom
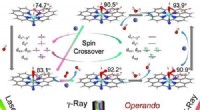
- Verrassende ontdekking kan de manier waarop de industrie nikkel gebruikt veranderen

- Directe synthese van waterstofperoxide met behulp van TS-1-ondersteunde katalysatoren
 Hoe worden de fysieke kenmerken van het kolen-vloeistofsysteem weerspiegeld in echografie?
Hoe worden de fysieke kenmerken van het kolen-vloeistofsysteem weerspiegeld in echografie? Wat is de oorsprong van magnetiet?
Wat is de oorsprong van magnetiet?  10 Feiten over weer en klimaat
10 Feiten over weer en klimaat  ASU werkt aan het redden van Hawaiiaanse koraalriffen tijdens het begin van een nieuwe hittegolf in de oceaan
ASU werkt aan het redden van Hawaiiaanse koraalriffen tijdens het begin van een nieuwe hittegolf in de oceaan Welke cel heeft een kern?
Welke cel heeft een kern?  Welke zone heeft in het binnenland een temperatuur hoger dan het smeltpunt?
Welke zone heeft in het binnenland een temperatuur hoger dan het smeltpunt?  Wat gebeurt er nadat een meteoor de maan raakt?
Wat gebeurt er nadat een meteoor de maan raakt?  Kwantumsystemen en de vlucht van de bij
Kwantumsystemen en de vlucht van de bij
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

