
Wetenschap
CO3^2- begrijpen:covalente versus ionische bindingen uitgelegd
* Ionische bindingen: Ionische bindingen vormen zich tussen een metaal en een niet-metaal. Het metaalatoom verliest elektronen om een positief geladen kation te worden, terwijl het niet-metaalatoom elektronen wint om een negatief geladen anion te worden. Deze tegengesteld geladen ionen worden door elkaar aangetrokken en vormen de ionische binding.
* Carbonaationenstructuur:
* Koolstof (C) is een niet-metaal.
*Zuurstof (O) is een niet-metaal.
* Het carbonaation (CO3^2-) wordt gevormd wanneer koolstof elektronen deelt met drie zuurstofatomen.
De bindingen binnen het carbonaation zijn echter feitelijk een mengsel van ionisch en covalent karakter.
* Covalent karakter: Koolstof en zuurstof delen elektronen op een covalente manier om de bindingen binnen het carbonaation te vormen. Vanwege de hoge elektronegativiteit van zuurstof brengen de gedeelde elektronen echter meer tijd door rond de zuurstofatomen, waardoor een gedeeltelijke negatieve lading op de zuurstofatomen ontstaat en een gedeeltelijke positieve lading op het koolstofatoom.
* Ionisch karakter: Deze ongelijke verdeling van elektronen leidt tot een algehele negatieve lading op het carbonaation, waardoor het een anion wordt.
Samengevat:
* Het carbonaation wordt bij elkaar gehouden door covalente bindingen in het ion zelf.
* Het carbonaation als geheel vormt ionische bindingen met andere positief geladen ionen in een verbinding.
Laat het me weten als je nog andere scheikundige vragen hebt!
 Zou een vlamtest werken om de specifieke stoffen te identificeren als ze meerdere kationen bevatten?
Zou een vlamtest werken om de specifieke stoffen te identificeren als ze meerdere kationen bevatten?  Ontleding door verhitting:welke verbindingen wel en niet kunnen worden afgebroken
Ontleding door verhitting:welke verbindingen wel en niet kunnen worden afgebroken  Waarom is zuurstof een gas?
Waarom is zuurstof een gas?  Waarom 80 procent aceton gebruiken als oplosmiddel bij de extractie van chlorofyl?
Waarom 80 procent aceton gebruiken als oplosmiddel bij de extractie van chlorofyl?  Hoe voorkom je oxidatie in een kogelmolen?
Hoe voorkom je oxidatie in een kogelmolen?
 Nieuwe tijdlijn voorgesteld voor platentektoniek
Nieuwe tijdlijn voorgesteld voor platentektoniek Hevige hittegolf treft herstel van overstromingen in Japan
Hevige hittegolf treft herstel van overstromingen in Japan Hoe burgerwetenschap passieve leerlingen transformeert in betrokken wetenschappers
Hoe burgerwetenschap passieve leerlingen transformeert in betrokken wetenschappers  Welke term omvat alle interactie die optreden tussen organisme en fysieke factoren in de vijveromgeving?
Welke term omvat alle interactie die optreden tussen organisme en fysieke factoren in de vijveromgeving?  Duizenden zoeken hun toevlucht terwijl grote hitte Groot-Brittannië teistert, Frankrijk
Duizenden zoeken hun toevlucht terwijl grote hitte Groot-Brittannië teistert, Frankrijk
Hoofdlijnen
- Wat is een schulling?
- Wetenschappers geven 's werelds eerste DNA-kaart van een bedreigde Australische muis vrij, en het zal helpen om deze te redden
- Waarom leven sommige microben in je darmen en andere niet?
- Is DNA-bewijs voldoende? Een interview met David Kaye
- Wat is chemosynthetisch organisme?
- Wat maakt een massa cellen met meer dan één celtype op?
- Hoe het Y-chromosoom de mannelijke ontwikkeling bij mensen stimuleert
- Wat is het trechtervormige deel van je oor dat wordt genoemd?
- Driehoekshoekberekeningen onder de knie krijgen:een stapsgewijze handleiding
- Fruitig met een vleugje schimmel:hoe schimmelinfecties het aroma van wijn veranderen

- Ultrahoge piëzo-elektrische prestaties aangetoond in keramische materialen
- Duurzaam, zeer selectieve biokatalytische omzetting van aldehyden in carbonzuren

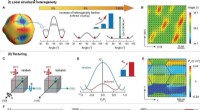
- Oplossen van molecuulinformatie in dynamisch lipidemembraan met meta-oppervlakken

- Vuurvliegjes werpen licht op de functie van mitochondriën
 Wat gebeurt er met de elektrische energie wanneer het door een huishoudelijk apparaat zoals blender of broodrooster gaat?
Wat gebeurt er met de elektrische energie wanneer het door een huishoudelijk apparaat zoals blender of broodrooster gaat?  Waarom krullen calla lily stelen in water?
Waarom krullen calla lily stelen in water?  Hoeveel cellen heeft het dier Kingdom?
Hoeveel cellen heeft het dier Kingdom?  Polyethyleenglycol versus ethyleenglycol:belangrijkste verschillen en veiligheidsinzichten
Polyethyleenglycol versus ethyleenglycol:belangrijkste verschillen en veiligheidsinzichten  Welke rol speelt RNA in genexpressie?
Welke rol speelt RNA in genexpressie?  Wat maakt de dubbele meteorenregen van 2024 tot een zeldzame hemelse gebeurtenis?
Wat maakt de dubbele meteorenregen van 2024 tot een zeldzame hemelse gebeurtenis?  Een obejct wordt naar het noorden getrokken met een kracht van 10 n en zuidwaarts 15 het magnitude net op object n?
Een obejct wordt naar het noorden getrokken met een kracht van 10 n en zuidwaarts 15 het magnitude net op object n?  Nieuwe LED's bieden mogelijk een betere manier om water in afgelegen gebieden te zuiveren
Nieuwe LED's bieden mogelijk een betere manier om water in afgelegen gebieden te zuiveren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

