
Wetenschap
De vorming van water begrijpen:zuurstof- en waterstofbinding
1. Elektronegativiteit: Zuurstof is aanzienlijk elektronegatiever dan waterstof. Dit betekent dat zuurstof een sterkere aantrekkingskracht uitoefent op gedeelde elektronen in een binding. Wanneer zuurstof en waterstof zich binden, brengen de elektronen meer tijd rond het zuurstofatoom door, waardoor het een gedeeltelijk negatieve lading krijgt en de waterstofatomen een gedeeltelijk positieve lading.
2. Octetregel: Zuurstof wil een volledige buitenschil van acht elektronen hebben. Het heeft zes elektronen in de buitenste schil. Door twee covalente bindingen te vormen met twee waterstofatomen, krijgt het nog twee elektronen, waardoor het octet wordt voltooid en stabiliteit wordt bereikt.
3. Waterstofbinding: Het resulterende watermolecuul heeft een gebogen vorm vanwege de losse elektronenparen op het zuurstofatoom. Hierdoor ontstaat een polair molecuul met een positieve kant (waterstofatomen) en een negatieve kant (zuurstofatoom). Deze tegengestelde ladingen zorgen ervoor dat watermoleculen sterke waterstofbruggen met elkaar kunnen vormen, wat leidt tot veel van de unieke eigenschappen van water.
4. Energievrijgave: Bij de vorming van water uit zuurstof en waterstof komt energie vrij, waardoor de reactie gunstig wordt.
Samengevat: De combinatie van de hoge elektronegativiteit van zuurstof, de wens om zijn octet te voltooien, de vorming van waterstofbruggen en het vrijkomen van energie dragen allemaal bij aan het gemak waarmee zuurstofatomen zich combineren met twee waterstofatomen om water te vormen.
Hoofdlijnen
- Welk type cel heeft het DNA in cel zwevend?
- Naast het kunnen groeien, wat is een ander voordeel van meercellig?
- Het proces waarin eukaryotische cellen zich verdelen?
- Atrazine verandert de sex-ratio in Blanchards krekelkikkers
- Waar worden enzymen geproduceerd binnen of buiten de cellen van een organisme?
- Wat gebeurt er als een enzym wordt renatureerd?
- Wat zijn groepen organen die samenwerken om een bepaalde baan in het lichaam te verrichten?
- Wat maakt aarde, aarde? Onderzoekers vinden verborgen aanwijzingen in DNA
- Segmenten van wat zijn overdracht van ouder tot nakomelingen genaamd genen?
- Gelijktijdige meting van biofysische eigenschappen en positie van afzonderlijke cellen in een microdevice

- Het aangaan van een 100 jaar oude uitdaging zou de weg kunnen banen naar digitale aroma's

- Converteren tussen moedervlekken, molariteit en volume:een praktische gids
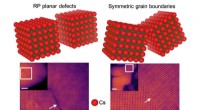
- Wanneer een defect gunstig kan zijn
- Onderzoek naar perovskiet-silicium tandemcellen laat nieuwe weg zien

 Biologen ontdekken hoe een kankerverwekkend virus de reactie van het immuunsysteem vermijdt
Biologen ontdekken hoe een kankerverwekkend virus de reactie van het immuunsysteem vermijdt  Optimalisatie van organische laagextractie met natriumcarbonaat
Optimalisatie van organische laagextractie met natriumcarbonaat  Nieuwe studie onthult dat gewoon keukenzout cruciaal kan zijn geweest voor het ontstaan van het leven
Nieuwe studie onthult dat gewoon keukenzout cruciaal kan zijn geweest voor het ontstaan van het leven De opkomst van microbiële valsspelers in ijzerarme omgevingen:onderzoek onthult hun evolutionaire geschiedenis
De opkomst van microbiële valsspelers in ijzerarme omgevingen:onderzoek onthult hun evolutionaire geschiedenis  Studie vindt geen versnelling in misdaad van Formule 1-race
Studie vindt geen versnelling in misdaad van Formule 1-race Ongeliefde Airbus A380's worden gestript voor onderdelen
Ongeliefde Airbus A380's worden gestript voor onderdelen CBS in gesprek over exit voor beschuldigde CEO Moonves:media
CBS in gesprek over exit voor beschuldigde CEO Moonves:media Russische natuurkundigen synthetiseren materialen voor het recyclen van radioactief afval
Russische natuurkundigen synthetiseren materialen voor het recyclen van radioactief afval
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


