
Wetenschap
Koper(II)sulfaat (CuSO₄):zuur of base? De eigenschappen ervan begrijpen
* Zout van een sterk zuur en een zwakke base: Koper(II)sulfaat is een zout dat ontstaat uit de reactie van een sterk zuur (zwavelzuur, H₂SO₄) en een zwakke base (koperhydroxide, Cu(OH)₂).
* Hydrolyse: Wanneer CuSO₄ oplost in water, ondergaat het hydrolyse, wat betekent dat de ionen reageren met watermoleculen. Het sulfaation (SO₄²⁻) reageert niet significant met water, maar het koper(II)-ion (Cu²⁺) wel. Het koper(II)-ion reageert met water en vormt hydroniumionen (H₃O⁺), waardoor de oplossing enigszins zuur wordt.
* pH: De pH van een CuSO₄-oplossing zal iets minder dan 7 zijn, wat wijst op een milde zuurgraad.
Samengevat:
* CuSO₄ is geen sterk zuur of sterke base.
* Het vertoont een milde zuurgraad als gevolg van de hydrolyse van het koper(II)-ion.
Het is echter belangrijk om te onthouden dat de zuurgraad van een CuSO₄-oplossing kan worden beïnvloed door factoren zoals concentratie en de aanwezigheid van andere chemicaliën.
 Sensoren gemaakt van bevroren rook kunnen giftig formaldehyde in huizen en kantoren detecteren
Sensoren gemaakt van bevroren rook kunnen giftig formaldehyde in huizen en kantoren detecteren  Wat gebeurt er als zilvernitraat reageert met ammoniumchloride?
Wat gebeurt er als zilvernitraat reageert met ammoniumchloride?  Hoe bewegen watermoleculen in hypotone oplossingen?
Hoe bewegen watermoleculen in hypotone oplossingen?  Geneesmiddelenresistentie bestrijden met snelle, kunstmatige verbetering van natuurlijke producten
Geneesmiddelenresistentie bestrijden met snelle, kunstmatige verbetering van natuurlijke producten Eigenschappen van thermische isolatoren
Eigenschappen van thermische isolatoren
 Monstercycloon Debbie treft noordoost Australië
Monstercycloon Debbie treft noordoost Australië Diepzee en sedimenten brengen ijzer naar de Antarctische wateren, vindt onderzoeker
Diepzee en sedimenten brengen ijzer naar de Antarctische wateren, vindt onderzoeker  Californië zal naar verwachting deze eeuw natter worden
Californië zal naar verwachting deze eeuw natter worden Welk bioom wordt gekenmerkt door lage temperaturen en hoeveelheden regenval?
Welk bioom wordt gekenmerkt door lage temperaturen en hoeveelheden regenval?  Afbeelding:Verlaten Venetiaanse lagune
Afbeelding:Verlaten Venetiaanse lagune
Hoofdlijnen
- Wat is proces dat moleculen over een celmembraan verplaatst van gebieden met een lagere concentratie naar hogere concentratie?
- Onderzoekers krijgen inzicht in hoe ultrakleine bacteriën uit de omgeving zich hebben aangepast om in mensen te leven
- Wat zijn de voordelen en nadelen van Flow Cytometry?
- Nee,
- Wat zijn enkele voorbeelden van gram -positieve bacteriën in de microbiologie?
- Waarom zou een wetenschapper de sequentie van DNA -molecuul willen weten?
- Wat is er allemaal betrokken bij de kern?
- Zijn insectieve planten en vleeseten hetzelfde?
- Wat is een verandering in de omgeving die een antwoordorganisme veroorzaakt?
- Succesvolle synthese van gamma-lactamringen uit koolwaterstoffen

- Enzym-aangedreven protocellen stijgen naar de top
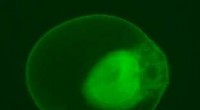
- Teamdetails plasmonisch effect waardoor de katalysator met lagere energie kan werken

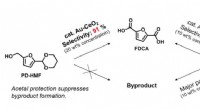
- Nieuwe methode maakt grootschalige productie van biobased plastic flessen mogelijk
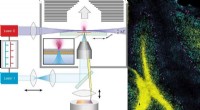
- Innovatieve methode geeft uniek inzicht in de structuur van cellen en weefsels
 Wat is het materiaal door welke licht reist als lucht of water?
Wat is het materiaal door welke licht reist als lucht of water?  Wat zijn alle sterren in Constellation Delphinus genoemd?
Wat zijn alle sterren in Constellation Delphinus genoemd?  Waarom worden cyanobacteriën als leden van de domeinbacteriën beschouwd?
Waarom worden cyanobacteriën als leden van de domeinbacteriën beschouwd?  Waarom vereisen transporteiwitten energie om te functioneren in actief transport?
Waarom vereisen transporteiwitten energie om te functioneren in actief transport?  Wat is het voorbeeld van magmatisme?
Wat is het voorbeeld van magmatisme?  Wanneer een object met een momentum van 80 kg x MS botsing -100, wat is het totale momentum?
Wanneer een object met een momentum van 80 kg x MS botsing -100, wat is het totale momentum?  Benchmarks om Som of Difference te schatten
Benchmarks om Som of Difference te schatten Hoe Light Pole Base Base
Hoe Light Pole Base Base
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

