
Wetenschap
Ionische versus covalente verbindingen:belangrijkste verschillen verklaard
1. Bondvorming:
* Ionisch: Gevormd door de overdracht van elektronen van een metaal naar een niet-metaal. Hierdoor ontstaan ionen met tegengestelde ladingen die elkaar sterk aantrekken en een elektrostatische binding vormen.
* Covalent: Gevormd door het delen van elektronen tussen twee niet-metalen. Deze gedeelde elektronen creëren een stabiele, meer gebalanceerde elektronenconfiguratie voor beide atomen.
2. Fysieke eigenschappen:
* Ionisch: Meestal vast bij kamertemperatuur met hoge smelt- en kookpunten . Dit komt omdat de sterke elektrostatische krachten veel energie vereisen om te overwinnen. Ze zijn vaak broos vanwege de stijve structuur van het kristalrooster.
* Covalent: Kan bestaan als vaste stoffen, vloeistoffen of gassen bij kamertemperatuur, afhankelijk van de specifieke verbinding. Hebben over het algemeen lagere smelt- en kookpunten dan ionische verbindingen. Ze kunnen flexibel zijn vanwege het zwakkere karakter van de obligaties.
3. Oplosbaarheid:
* Ionisch: Vaak oplosbaar in water vanwege de polaire aard van watermoleculen die kunnen interageren met de geladen ionen.
* Covalent: Varieren in oplosbaarheid , waarbij sommige oplosbaar zijn in water (bijvoorbeeld suikers) en andere onoplosbaar zijn (bijvoorbeeld oliën). De oplosbaarheid hangt af van de polariteit van het molecuul en het vermogen van de watermoleculen om waterstofbruggen te vormen.
Samengevat: Ionische verbindingen worden gevormd door de overdracht van elektronen, zijn meestal vast en sterk en lossen goed op in water. Covalente verbindingen worden gevormd door het delen van elektronen, kunnen in verschillende toestanden voorkomen, hebben zwakkere bindingen en vertonen een variërende oplosbaarheid in water.
 Australische steden op de heetste plekken op aarde terwijl de hittegolf sist
Australische steden op de heetste plekken op aarde terwijl de hittegolf sist Wetenschappers onderzoeken hoe verschillende huizen en levensstijlen van invloed zijn op welke insecten bij ons leven
Wetenschappers onderzoeken hoe verschillende huizen en levensstijlen van invloed zijn op welke insecten bij ons leven  Colombia verbiedt sportjacht
Colombia verbiedt sportjacht Niet alle zeevissen eten plastic
Niet alle zeevissen eten plastic Er is meer nodig dan goede bedoelingen om de afvalbergen van Nairobis op te ruimen
Er is meer nodig dan goede bedoelingen om de afvalbergen van Nairobis op te ruimen
Hoofdlijnen
- Welke uitspraken beschrijven wetenschappers het beste die bijdragen aan het huidige geheel van wetenschappelijke kennis?
- Waarom het leren van dierengeluiden cruciaal kan zijn voor de taalontwikkeling van kinderen
- Wat is diffusie in de biologie?
- Wat transporteert een planten vasculair systeem?
- 520 miljoen jaar oud wormfossiel lost het mysterie op van hoe moderne insecten, spinnen en krabben zijn geëvolueerd
- Waarom is het belangrijk dat planten celwanden laten hint, skeletten?
- Welke tak van de wetenschap is afdrukken?
- Wat zijn twee menselijke activiteiten die bijdragen aan de globale wording?
- Welke hersenstructuur maakt deel uit van het endocriene systeem?
- Uit een spaghetti-achtige wirwar van microvezels en water komt een veelbelovend nieuw materiaal

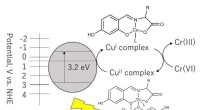
- Reductie door reductie:nieuwe aanpak om chroomverontreiniging in afvalwater te verminderen
- Een virtueel substraat opent de weg naar oxidefilms op silicium voor toepassing in 5G, MEMS, sensoren en kwantumberekening

- Onderzoekers voltooien het eerste Britse onderzoek naar synthetische chemicaliën in voedsel

- Nieuwe studie identificeert mogelijke voorouders van RNA

 Boeing rondt anti-stall-update af na crash in Ethiopië
Boeing rondt anti-stall-update af na crash in Ethiopië Hoe snel vindt de evolutie plaats?
Hoe snel vindt de evolutie plaats?  Waarom worden inductoren niet gebruikt in geïntegreerde circuits?
Waarom worden inductoren niet gebruikt in geïntegreerde circuits?  Inzicht in de atomaire structuur:protonen, neutronen en elektronen
Inzicht in de atomaire structuur:protonen, neutronen en elektronen  Koolstofafvang kan een financiële kans zijn voor Amerikaanse biobrandstoffen
Koolstofafvang kan een financiële kans zijn voor Amerikaanse biobrandstoffen Wanneer de temperatuur van een gas bewegingsdeeltjes verhoogt?
Wanneer de temperatuur van een gas bewegingsdeeltjes verhoogt?  Welk organisme verkrijgt zijn energie uit dode of rottende materie?
Welk organisme verkrijgt zijn energie uit dode of rottende materie?  Mayweath zal McGregor verslaan, neurowetenschap voorspelt
Mayweath zal McGregor verslaan, neurowetenschap voorspelt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

