
Wetenschap
Waterstofchloride (HCl):covalent karakter uitgelegd
Dit is waarom:
* Elektronegativiteit: Chloor is veel elektronegatiever dan waterstof. Dit betekent dat chloor een sterkere aantrekkingskracht uitoefent op de gedeelde elektronen in de binding. Hoewel de binding niet perfect gelijk is, is het geen volledige overdracht van elektronen zoals bij een ionische binding.
* Polair covalent: Door de ongelijke verdeling van elektronen ontstaat een gedeeltelijk positieve lading op waterstof (δ+) en een gedeeltelijk negatieve lading op chloor (δ-). Dit maakt HCl een polair covalent molecuul.
* Gastoestand: Bij kamertemperatuur is HCl een gas, typisch voor covalente verbindingen. Ionische verbindingen daarentegen vormen gewoonlijk vaste kristallen bij kamertemperatuur.
Samengevat: Hoewel HCl een bepaald ionisch karakter vertoont vanwege het verschil in elektronegativiteit, wordt het voornamelijk geclassificeerd als een covalente verbinding vanwege het delen van elektronen en de gasvormige toestand ervan.
 Welk type chemische binding zou u verwachten tussen een calciumatoom Ca Atomic aantal twintig en chloor CL zeventien?
Welk type chemische binding zou u verwachten tussen een calciumatoom Ca Atomic aantal twintig en chloor CL zeventien?  Prijs van gegalvaniseerd staal versus Roestvrij staal
Prijs van gegalvaniseerd staal versus Roestvrij staal Een neutraal atoom heeft altijd wat?
Een neutraal atoom heeft altijd wat?  PFAS-chemicaliën gaan niet eeuwig mee
PFAS-chemicaliën gaan niet eeuwig mee Welke term wordt gedefinieerd als proces waardoor een stofverandering van staet van vaste tot vloeistof verandert?
Welke term wordt gedefinieerd als proces waardoor een stofverandering van staet van vaste tot vloeistof verandert?
Hoofdlijnen
- Wat blozen onthult over uw zenuwstelsel
- Hoe ontwikkelen pathogenen nieuwe virulentie-activiteiten, en waarom doet dat ertoe?
- Hoe beïnvloedt polyploïdie dieren mens en planten?
- Hoe komen de spermacellen in een stuifmeelkorrel aan bij de eicelklus in een plant-ovule?
- In welke relatie profiteren beide soorten?
- Wat is een enkele celfunctie?
- Chromosomale afwijkingen: wat is het?, Typen en oorzaken
- "What Does Heterozygous Mean?
- Wat zijn de twee soorten coördinatie in levende organismen?
- Vooruitgang in jacht op onbekende verbindingen in drinkwater

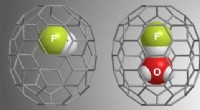
- Onderzoekers isoleren waterstoffluoride en water om zuuroplossing te begrijpen
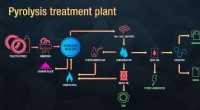
- Verspil niet, want not:een zelf ontwikkeld plan om van plastic en banden brandstof te maken
- Biostasis heeft tot doel de dood na traumatisch letsel te voorkomen door biochemische reacties in cellen te vertragen

- Nieuwe topologische materialen kunnen meerdere elektrische eigenschappen hebben

 Wat zijn de zes brede typen van klimaatregio's?
Wat zijn de zes brede typen van klimaatregio's?  Wat hebben planten nodig om hun eigen voedsel en energie te maken?
Wat hebben planten nodig om hun eigen voedsel en energie te maken?  Hoge niveaus van PFOA gevonden bij inwoners van midden Ohio River Valley van 1991 tot 2013
Hoge niveaus van PFOA gevonden bij inwoners van midden Ohio River Valley van 1991 tot 2013 Water bestaat uit deeltjes genaamd?
Water bestaat uit deeltjes genaamd?  Geef een voorbeeld van energieconversie die ongewenste vormen van energie produceert?
Geef een voorbeeld van energieconversie die ongewenste vormen van energie produceert?  Hoe wordt kalksteen gebruikt om de bodemvruchtbaarheid te verbeteren?
Hoe wordt kalksteen gebruikt om de bodemvruchtbaarheid te verbeteren?  Wat hebben plantencellen dat dier niet?
Wat hebben plantencellen dat dier niet?  Wat is de golflengte van 10 Hz?
Wat is de golflengte van 10 Hz?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

