
Wetenschap
Periode 3 Elementen en oplosbaarheid in hexaan:een gedetailleerde uitleg
De oplosbaarheid in hexaan begrijpen
Hexaan (C6H14) is een niet-polair oplosmiddel. Dit betekent dat het stoffen oplost die ook niet-polair zijn of een niet-polaire component hebben. Hier ziet u hoe de oplosbaarheid van elementen uit periode 3 verband houdt met dit principe:
* Natrium (Na), Magnesium (Mg), Aluminium (Al): Dit zijn metalen en vormen ionische verbindingen. Ionische verbindingen zijn polair, waardoor ze onoplosbaar zijn in hexaan.
* Silicium (Si): Silicium is een metalloïde en bestaat als een netwerkvaste stof. Hoewel het enige covalente bindingen heeft, wordt het voornamelijk bij elkaar gehouden door sterke interatomaire krachten. Dit maakt het onoplosbaar in hexaan.
* Fosfor (P), Zwavel (S), Chloor (Cl): Deze elementen kunnen niet-polaire covalente verbindingen vormen. Enkele voorbeelden:
* Witte fosfor (P4) is een niet-polair molecuul en oplosbaar in hexaan.
* Elementaire zwavel (S8) is enigszins oplosbaar in hexaan.
* Chloor (Cl2) is een niet-polair diatomisch molecuul en oplosbaar in hexaan.
Belangrijke overwegingen
* Oxidatietoestanden: De oplosbaarheid van een element kan veranderen afhankelijk van de oxidatietoestand ervan. Zwavel in zijn elementaire vorm (S8) is bijvoorbeeld enigszins oplosbaar, maar zwavel in zijn oxidevormen (zoals SO2) is polair en onoplosbaar in hexaan.
* Specifieke verbindingen: De oplosbaarheid van specifieke verbindingen die elementen uit periode 3 bevatten, zal afhangen van de structuur en polariteit van het gehele molecuul.
Samengevat: Elementen in periode 3 die niet-polaire covalente verbindingen vormen, zijn waarschijnlijk oplosbaar in hexaan. Metalen, metalloïden en ionische verbindingen zijn over het algemeen onoplosbaar.
 Ontdooiende permafrost zit vol ijsvormende deeltjes die in de atmosfeer kunnen komen
Ontdooiende permafrost zit vol ijsvormende deeltjes die in de atmosfeer kunnen komen MBL-team fotografeert de bacteriële lifters op plastic afval in de oceaan
MBL-team fotografeert de bacteriële lifters op plastic afval in de oceaan Een onderzeese vulkaan ontdekt in de buurt van Christmas Island lijkt op het oog van Sauron
Een onderzeese vulkaan ontdekt in de buurt van Christmas Island lijkt op het oog van Sauron Hoe reinigt de natuur zijn eigen water?
Hoe reinigt de natuur zijn eigen water?  Feiten over Owl Pellets
Feiten over Owl Pellets
Hoofdlijnen
- Wat bevat het ruwe endoplasmatische materiaal dat het gladde reticulum niet heeft?
- Welke uitspraken zijn waar voor alle wetenschappelijke inspanningen?
- Is biopolair een aandoening waarmee u wordt geboren of wordt deze geërfd?
- Wat gebeurt er met de cellen van groenten en fruit als ze voldoende water krijgen?
- Als je Google het woord vinkje gebruikt, help je de wetenschap
- Waar bevinden de genen zich?
- Wat doet mitochondriën in plantencellen voor celademhaling?
- Wat zijn de meest primitieve organismen die tegenwoordig een structuur hebben die te simpel is als cellen.?
- Welk deel van de cel stuurt alle activiteiten op?
- Het oplossen van een fossiel mysterie kan de zoektocht naar het leven op Mars helpen
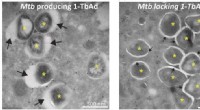
- Antacida helpt tuberculosebacteriën te overleven
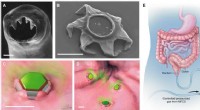
- Gastro-intestinaal-bewoner, vormveranderende microdevices voor verlengde medicijnafgifte
- Deponeren van ijzersoorten in ZSM-5 om cyclohexaan te oxideren tot cyclohexanon

- Wetenschappers hebben nieuwe verbindingen met mogelijk antitumoreffect verkregen uit zeespons

 Hoeveel totale zuurstofatomen 2CO2 en 3 H2O gecombineerd?
Hoeveel totale zuurstofatomen 2CO2 en 3 H2O gecombineerd?  EasyJet wordt geraakt door drone-chaos van Londense luchthaven
EasyJet wordt geraakt door drone-chaos van Londense luchthaven Wat gebeurt er zwaartekracht van aantrekkingskracht tussen twee object als massa één wordt gehalveerd?
Wat gebeurt er zwaartekracht van aantrekkingskracht tussen twee object als massa één wordt gehalveerd?  Hoeveel gallons zijn er in 5300 liter?
Hoeveel gallons zijn er in 5300 liter?  Wat zijn de voor- en nadelen van diodelasers?
Wat zijn de voor- en nadelen van diodelasers?  Kun je correct zeggen dat een nieuwe energiebron waterstof is?
Kun je correct zeggen dat een nieuwe energiebron waterstof is?  Is een kalksteengesteente of mineraal?
Is een kalksteengesteente of mineraal?  Robots kunnen worden gebruikt om het mentale welzijn van kinderen te beoordelen, suggereert onderzoek
Robots kunnen worden gebruikt om het mentale welzijn van kinderen te beoordelen, suggereert onderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

