
Wetenschap
Kookpuntvergelijking:2-methyl-1-buteen versus 1-penteen - Chemie uitgelegd
Vertakking en kookpunt
* Vertakking verlaagt het kookpunt: Vertakte alkanen hebben lagere kookpunten dan hun isomeren met rechte keten. Dit komt omdat vertakkingen het oppervlak verkleinen dat beschikbaar is voor intermoleculaire krachten (zoals Londense dispersiekrachten) om op in te werken.
Vergelijking van 2-methyl-1-buteen en 1-penteen
* 1-penteen: Een alkeen met een rechte keten en een groter oppervlak.
* 2-methyl-1-buteen: Een vertakt alkeen met een kleiner oppervlak doordat de methylgroep zich vertakt van de hoofdketen.
Conclusie
Omdat 1-penteen een groter oppervlak heeft, ervaart het sterkere intermoleculaire krachten, waardoor er meer energie nodig is om deze krachten te overwinnen en over te gaan naar de gasfase. Dit resulteert in een hoger kookpunt vergeleken met 2-methyl-1-buteen.
Laat het me weten als je nog vragen hebt!
 De pH van een 0,01 m oplossing natriumacetaat berekenen?
De pH van een 0,01 m oplossing natriumacetaat berekenen?  Typen lijm gebruikt in OSB
Typen lijm gebruikt in OSB  Welke test kan het beste worden gebruikt om een niet-metaalachtig mineraal van metallisch mineraal te onderscheiden?
Welke test kan het beste worden gebruikt om een niet-metaalachtig mineraal van metallisch mineraal te onderscheiden?  Wat zijn de drie gemeenschappelijke verbindingen van Neptunium?
Wat zijn de drie gemeenschappelijke verbindingen van Neptunium?  Een nieuwe gouden eeuw voor elektronica?
Een nieuwe gouden eeuw voor elektronica?
 Hoe zijn bos nuttig voor de mens?
Hoe zijn bos nuttig voor de mens?  Natuurlijke afzettingen van heliumgas kunnen helpen bij de veilige productie van schalie- of steenkoolgas, onderzoek suggereert:
Natuurlijke afzettingen van heliumgas kunnen helpen bij de veilige productie van schalie- of steenkoolgas, onderzoek suggereert: Mensen hebben de afgelopen 35 jaar minstens 250.000 hectare aan riviermondingen omgebouwd tot steden en boerderijen, zo blijkt uit onderzoek
Mensen hebben de afgelopen 35 jaar minstens 250.000 hectare aan riviermondingen omgebouwd tot steden en boerderijen, zo blijkt uit onderzoek  Oceaanwetenschappers meten sedimentpluim die wordt opgewekt door diepzeemijnbouwvoertuig
Oceaanwetenschappers meten sedimentpluim die wordt opgewekt door diepzeemijnbouwvoertuig Duitse chemische industrie schetst kostbaar CO2-neutraal pad
Duitse chemische industrie schetst kostbaar CO2-neutraal pad
Hoofdlijnen
- Wat is grafiek in de wetenschap?
- Een decomposer is een insectenschimmel of bacteriën die dierenplanten breekt?
- Wat is het principe -enzym dat betrokken is bij DNA -replicatie?
- Wat zijn 3 soorten bewijs voor evolutie?
- De menselijke huid was beter bestand tegen de zon voordat er zonneschermen en parasols waren. Een antropoloog legt uit waarom
- Wat is de wetenschappelijke naam van de massa?
- De levenscyclus van een rozenplant
- Wat zijn de regels van het basispaar voor nucleotiden CGTA?
- Wat voor soort organisme is bacteriën?
- Fysica van ladingstransport van een unieke klasse van geconjugeerde polymeren met stijve staven
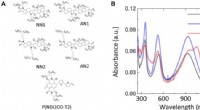
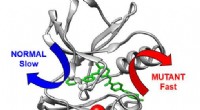
- Computersimulaties van eiwitten helpen te ontrafelen waarom resistentie tegen chemotherapie optreedt
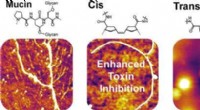
- Synthetisch slijm kan het echte werk nabootsen
- Apparaat verbindt metaal en plastic binnen enkele seconden

- Wat u moet weten over chemische verbindingen

 Is diarseenpentoxide ionisch of covalent?
Is diarseenpentoxide ionisch of covalent?  Top VW-aandeelhouder geconfronteerd met woede van investeerders in eigen dieselgate-pak
Top VW-aandeelhouder geconfronteerd met woede van investeerders in eigen dieselgate-pak De plaats waar lichte reacties optreden in een plant?
De plaats waar lichte reacties optreden in een plant?  Celwandsamenstelling in de zes biologische koninkrijken
Celwandsamenstelling in de zes biologische koninkrijken  Onderzoekers vergroten het inzicht in waarom celonderdelen er zo uitzien zoals ze eruitzien
Onderzoekers vergroten het inzicht in waarom celonderdelen er zo uitzien zoals ze eruitzien  Een natuurkunde -leraar wrijft een glasobject en voelde doek samen en wordt positief geladen. Welke van de volgende uitspraken zijn waar?
Een natuurkunde -leraar wrijft een glasobject en voelde doek samen en wordt positief geladen. Welke van de volgende uitspraken zijn waar?  Hoe worden gegevens gebruikt in de wetenschappelijke methode?
Hoe worden gegevens gebruikt in de wetenschappelijke methode?  Is de afwezigheid van diepe focus aardbevingen langs het oceanische noksysteem niet consistent met theorieplaattektoniek?
Is de afwezigheid van diepe focus aardbevingen langs het oceanische noksysteem niet consistent met theorieplaattektoniek?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

