
Wetenschap
Nuclidenotatie en ionen begrijpen:waarom zwavelionen ze niet hebben
* Nuclidenotatie: Nuclidennotatie is een manier om specifieke isotopen van een element weer te geven. Het gebruikt het volgende formaat:
* ^A_ZX
* Een is het massagetal (protonen + neutronen)
* Z is het atoomnummer (aantal protonen)
* X is het elementsymbool
* Ionen- en nuclidennotatie: Ionen zijn atomen die elektronen hebben gewonnen of verloren, waardoor hun lading verandert. Het aantal protonen en neutronen (die het massagetal en het atoomnummer bepalen) blijft echter hetzelfde.
Daarom vertegenwoordigt de nuclidennotatie de kern van een atoom, die niet wordt beïnvloed door de winst of het verlies van elektronen.
Voorbeeld:
* Zwavel (S) heeft 16 protonen en heeft doorgaans 16 neutronen (hoewel er verschillende isotopen bestaan). De meest voorkomende nuclidennotatie is ^32_16S .
* Sulfide-ion (S^2-) heeft er twee elektronen bij gekregen, maar de kern blijft hetzelfde. De nuclidennotatie is nog steeds ^32_16S .
Samengevat: De nuclidennotatie beschrijft de samenstelling van de kern, die niet wordt beïnvloed door de vorming van ionen.
 Waarom bepaalt de hoeveelheid gebruikte waterstofperoxide hoe licht je haarkleur is?
Waarom bepaalt de hoeveelheid gebruikte waterstofperoxide hoe licht je haarkleur is?  Van spoor wisselen:Omgekeerde elektronen gaan door natuurlijke zonnecellen
Van spoor wisselen:Omgekeerde elektronen gaan door natuurlijke zonnecellen Wat veroorzaakt oxidatie van smeerolie?
Wat veroorzaakt oxidatie van smeerolie?  Er zijn moleculen van lucht op hoog, dus is de druk minder?
Er zijn moleculen van lucht op hoog, dus is de druk minder?  Van welk orbitaal in een lithiumatoom is een elektron overgedragen om een positief ion te maken?
Van welk orbitaal in een lithiumatoom is een elektron overgedragen om een positief ion te maken?
Hoofdlijnen
- Bestaan alle levende organismen uit cellen?
- Wiens systeem van klasse en het benoemen van organismen is vandaag nog steeds in gebruik?
- Waar zijn giste en suboptimale voorbeelden van?
- Walvissen en dolfijnen hebben rijke mensachtige culturen en samenlevingen
- Welke natuurlijke selectie noemde extreem fenotype?
- Waar bevindt het celmembraan zich in een plantencel?
- Bewaakt een celwand voedsel en water in cel?
- Biosfeer uitgelegd:definitie, hulpbronnen, cycli, feiten en voorbeelden uit de echte wereld
- Wat is een witte neushoorn herbivoor omnivore of carnivoor?
- Pentaceenderivaat heeft 100 keer meer lichtbestendigheid dan conventionele producten

- Onderzoekers ontwikkelen zich snel, efficiënte manier om aminozuurketens te bouwen

- De grenzen van kooldioxidefixatie verleggen
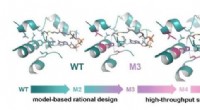
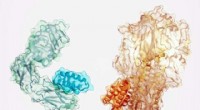
- Nieuwe methode voor het genereren van krachtige, specifieke bindende eiwitten voor nieuwe medicijnen
- Een vereenvoudigd nieuw proces zet houtafval uit landbouw en bosbeheer om in ethanol

 Hoe transformeren cellen uit het uitscheidingssysteem in organen?
Hoe transformeren cellen uit het uitscheidingssysteem in organen?  Naam van de vloeistof in het menselijk oor?
Naam van de vloeistof in het menselijk oor?  Uit voedingsonderzoek blijkt dat begrafenismaaltijden van mensen in het Romeinse rijk bijna hetzelfde zijn als dagelijkse maaltijden
Uit voedingsonderzoek blijkt dat begrafenismaaltijden van mensen in het Romeinse rijk bijna hetzelfde zijn als dagelijkse maaltijden Onderzoekers onderzoeken de invloed van schimmelrot op de aroma's van most en wijn
Onderzoekers onderzoeken de invloed van schimmelrot op de aroma's van most en wijn GMs Cruise gaat nieuwe weg in met nieuw robotaxi-concept
GMs Cruise gaat nieuwe weg in met nieuw robotaxi-concept Energiegebruiksgedrag beïnvloeden door training en gamification
Energiegebruiksgedrag beïnvloeden door training en gamification Hoe vind je de massa onregelmatig object tonen experiment?
Hoe vind je de massa onregelmatig object tonen experiment?  Nieuw 3D-printproces biedt nieuwe ontwerpopties voor energieopslag
Nieuw 3D-printproces biedt nieuwe ontwerpopties voor energieopslag
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

