
Wetenschap
Waterstofproductie uit water:een uitgebreide gids
Het proces:
1. Elektrolyse: Water wordt door een elektrolytische cel geleid die twee elektroden (anode en kathode) bevat, ondergedompeld in een elektrolytoplossing (meestal een base zoals kaliumhydroxide of natriumhydroxide).
2. Gelijkstroomtoepassing: Er wordt een gelijkstroom (DC) over de elektroden aangelegd, waardoor een potentiaalverschil ontstaat.
3. Waterafbraak: De toegepaste elektriciteit zorgt ervoor dat de watermoleculen uiteenvallen in hun samenstellende elementen:waterstof (H2) en zuurstof (O2).
4. Waterstofverzameling: Aan de kathode (negatieve elektrode) wordt waterstofgas geproduceerd en opgevangen.
5. Zuurstofverzameling: Zuurstofgas wordt geproduceerd aan de anode (positieve elektrode) en kan ook worden opgevangen.
Chemische reactie:
De totale reactie tijdens elektrolyse kan worden weergegeven als:
2H2O(l) → 2H2(g) + O2(g)
Belangrijkste punten:
* Energie-input: Elektrolyse vereist een aanzienlijke energie-input om de bindingen in watermoleculen te verbreken. Deze energie is meestal afkomstig van hernieuwbare bronnen zoals zonne- of windenergie, om het proces echt duurzaam te maken.
* Elektrolyt: De elektrolytoplossing helpt elektriciteit te geleiden en vergemakkelijkt de beweging van ionen tijdens het elektrolyseproces.
* Zuiverheid: De waterstof die door elektrolyse wordt geproduceerd, is doorgaans zeer zuiver, omdat deze rechtstreeks van water wordt gescheiden.
* Groene waterstof: Wanneer de elektriciteit die wordt gebruikt voor elektrolyse afkomstig is uit hernieuwbare bronnen, wordt de geproduceerde waterstof beschouwd als 'groene waterstof', die een schoon alternatief biedt voor waterstof uit fossiele brandstoffen.
Andere methoden:
Hoewel elektrolyse de meest gebruikelijke methode is, omvatten andere technieken voor de productie van waterstof uit water:
* Thermochemische processen: Hierbij gaat het om chemische reacties bij hoge temperaturen om watermoleculen te splitsen, vaak met behulp van geconcentreerde zonne-energie.
* Foto-elektrochemische processen: Deze gebruiken halfgeleidermaterialen om zonlicht direct om te zetten in elektriciteit, die vervolgens het elektrolyseproces aandrijft.
Uitdagingen:
* Energie-efficiëntie: Elektrolyse kan energie-intensief zijn en een aanzienlijke elektriciteitsinput vereisen.
* Kosten: De kosten voor het produceren van waterstof door middel van elektrolyse kunnen hoger zijn in vergelijking met andere methoden, vooral als je de elektriciteitskosten in ogenschouw neemt.
* Opschalen: Het opschalen van de elektrolyseproductie om aan de grootschalige vraag te voldoen vereist vooruitgang in technologie en infrastructuur.
Over het geheel genomen houdt de waterstofproductie uit water door middel van elektrolyse een grote belofte in voor een schonere energietoekomst, maar technologische vooruitgang en kostenbesparingen zijn nog steeds cruciaal voor de wijdverbreide toepassing ervan.
 Wat is het verschil tussen rood ijzeroxide en zwart oxide?
Wat is het verschil tussen rood ijzeroxide en zwart oxide?  Natrium heeft één elektron in zijn buitenste schaal volgens de octetregel?
Natrium heeft één elektron in zijn buitenste schaal volgens de octetregel?  Waarom is regen natuurlijk zuur?
Waarom is regen natuurlijk zuur?  Wat zou de lading van zuurstof zijn als het ioniseert?
Wat zou de lading van zuurstof zijn als het ioniseert?  Het chlooratoom heeft 7 elektronen in zijn buitenste schaal 8 zal het stabiel maken wat moet stabiel worden?
Het chlooratoom heeft 7 elektronen in zijn buitenste schaal 8 zal het stabiel maken wat moet stabiel worden?
 Dieren naast mensen die houden van plezier
Dieren naast mensen die houden van plezier  Kunnen symbiotische microben ecosystemen helpen de opwarming van de aarde te overleven?
Kunnen symbiotische microben ecosystemen helpen de opwarming van de aarde te overleven? Wat is de oorzaak van een storm en hoe werkt deze?
Wat is de oorzaak van een storm en hoe werkt deze?  Wetenschappers proberen wolken helderder te maken om het Great Barrier Reef te beschermen
Wetenschappers proberen wolken helderder te maken om het Great Barrier Reef te beschermen Verontreiniging door tankstations
Verontreiniging door tankstations
Hoofdlijnen
- Wat zijn voorbeelden van estivatie?
- Wat gebruiken organismen om te werken en veranderen?
- Hoe is een dierlijke voedselketen in het tropische regenwoud?
- Waarom vereist osmose een semipermeabiel membraan?
- Welke factor kan naast zuurstof de groei van verschillende typen bacteriën beïnvloeden?
- Meerdere stressoren kunnen interactief leiden tot verslechtering van aquatische ecosystemen
- Wat kunnen veranderingen in de fossielen van een enkel organisme in de loop van de tijd onthullen?
- Biologische evolutie begrijpen:een uitgebreide gids
- Wat zijn de daar genoemde punten van de celtheorie?
- Dwazen goud kan toch waardevol zijn

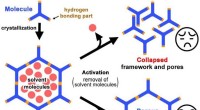
- Poreuze materialen werpen licht op milieuzuivering
- Nieuwe aanpak maakt het gemakkelijker om nieuwe medicijnen te vinden
- Berekening van de pH van een ammoniakoplossing met behulp van de base-dissociatieconstante (Kb)

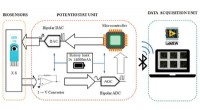
- Bluetooth-apparaat detecteert het fermentatieproces gedurende dagen
 Waar wordt Brookite gevonden?
Waar wordt Brookite gevonden?  Donkere luchten beschermen voor astronomie en leven
Donkere luchten beschermen voor astronomie en leven Wat is een vergelijking voor genotype?
Wat is een vergelijking voor genotype?  Hoe op te lossen voor X in een Trianlge
Hoe op te lossen voor X in een Trianlge  Kunnen intensievere landbouwpraktijken ten goede komen aan tropische vogels?
Kunnen intensievere landbouwpraktijken ten goede komen aan tropische vogels?  Een simpele snuif:onderzoek naar nanodeeltjes getest in sprinkhanen richt zich op nieuwe methode voor medicijnafgifte
Een simpele snuif:onderzoek naar nanodeeltjes getest in sprinkhanen richt zich op nieuwe methode voor medicijnafgifte Heeft elk stationair lichaam potentiële energie?
Heeft elk stationair lichaam potentiële energie?  Hoe de thermische energie van koelvloeistof verandert als deze in een koelkast stroomt?
Hoe de thermische energie van koelvloeistof verandert als deze in een koelkast stroomt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

