
Wetenschap
Graham's wet van effusie:molaire massa en gassnelheid
Deze relatie staat bekend als de wet van effusie van Graham :
```
Tarief₁ / Tarief₂ =√(M₂ / M₁)
```
Waar:
* Tarief₁ is de effusiesnelheid van gas 1
* Tarief₂ is de effusiesnelheid van gas 2
* M₁ is de molaire massa van gas 1
* M₂ is de molaire massa van gas 2
Uitleg:
De effusiesnelheid wordt bepaald door de gemiddelde snelheid van de gasmoleculen. Lichtere moleculen bewegen sneller dan zwaardere moleculen bij dezelfde temperatuur. Dit komt omdat de kinetische energie van een gasmolecuul evenredig is met zijn temperatuur en zijn massa.
Daarom hebben lichtere moleculen een hogere gemiddelde snelheid en stromen ze dus sneller door een kleine opening.
Voorbeeld:
Denk aan helium (He) en zuurstof (O₂). Helium heeft een molmassa van 4 g/mol, terwijl zuurstof een molmassa heeft van 32 g/mol.
Volgens de wet van Graham:
```
Tarief(He) / Tarief(O₂) =√(32 / 4) =√8 ≈ 2,83
```
Dit betekent dat helium ongeveer 2,83 keer sneller uitstraalt dan zuurstof.
Toepassingen:
De wet van Graham heeft verschillende toepassingen in de scheikunde en natuurkunde, waaronder:
* Gassen scheiden: Gassen met verschillende molmassa's kunnen worden gescheiden door ze door een poreus membraan te laten stromen.
* Mole massa bepalen: De molaire massa van een onbekend gas kan worden bepaald door de effusiesnelheid ervan te vergelijken met die van een bekend gas.
* Inzicht in gasdiffusie: Het concept van de effusiesnelheid houdt ook verband met de diffusie van gassen, wat de beweging is van gasmoleculen van een gebied met een hoge concentratie naar een gebied met een lage concentratie.
 Waarom heb je ecosystemen?
Waarom heb je ecosystemen?  Hoe is het klimaat aan de Leeward -kant van een berg verschilt van die windwaartse kant?
Hoe is het klimaat aan de Leeward -kant van een berg verschilt van die windwaartse kant?  Typen Arizona wilde katten
Typen Arizona wilde katten  Nieuwe interactieve scenarioverkenner voor 1,5 graden C-paden
Nieuwe interactieve scenarioverkenner voor 1,5 graden C-paden Sommige gemeenschappen zijn kwetsbaarder voor weersgerelateerde stroomstoringen in de staat New York
Sommige gemeenschappen zijn kwetsbaarder voor weersgerelateerde stroomstoringen in de staat New York
Hoofdlijnen
- Ornithologen ontdekken dat 's werelds grootste kolibrie eigenlijk uit twee soorten bestaat
- Zijn mannelijke genen van Mars, vrouwelijke Venus? Review benadrukt sekseverschillen in gezondheid en ziekte
- Wat betekent Crocodylidae?
- Hoe werken dominante en recessieve genen?
- Wat is een mitochondira?
- Welke klasse van enzymen hoort Lactase te zijn?
- Onderzoekers tonen aan dat RNA-ribozymen in staat zijn om samen te werken en zichzelf weer in elkaar te zetten
- Wat is de naam van het proces waarin bacteriën en bliksem stikstof omzetten in verbindingen die nuttig zijn voor planten?
- Hoe planten hun zaden vormen
- Ultra-efficiënte verwijdering van koolmonoxide met behulp van gouden nanodeeltjes op een moleculaire drager
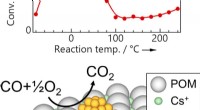
- Nieuwe zenuwgasdetector gebouwd met lego's en een smartphone

- Nieuw model voor bimoleculaire reacties in nanoreactoren
- Ontdekking van een universeel systeem voor het transporteren van nucleïnezuren in cellen
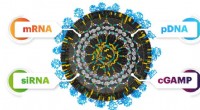
- Onderzoekers ontwikkelen met goud gecomplexeerde ferrocenylfosfines als krachtige antimalariamiddelen
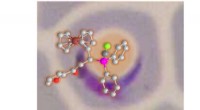
 Jet Airways-geldschieters stappen naar de faillissementsrechtbank
Jet Airways-geldschieters stappen naar de faillissementsrechtbank Heroverweging van lichaamswerelden:waarom komen we nog steeds massaal naar tentoonstellingen van dode mensen?
Heroverweging van lichaamswerelden:waarom komen we nog steeds massaal naar tentoonstellingen van dode mensen?  Waar zijn de chromosomen van de meeste organismen gevestigd?
Waar zijn de chromosomen van de meeste organismen gevestigd?  Welke twee structuren passeren water en mineralen om xyleem te krijgen?
Welke twee structuren passeren water en mineralen om xyleem te krijgen?  Commentaarsectie van YouTube:politieke echokamer of constructief partijoverschrijdend forum?
Commentaarsectie van YouTube:politieke echokamer of constructief partijoverschrijdend forum?  Door de zee van Galilea, Archeologen vinden ruïnes van vroege moskee
Door de zee van Galilea, Archeologen vinden ruïnes van vroege moskee Eerste celkaart van 20, 000 cellen in zoogdierembryo
Eerste celkaart van 20, 000 cellen in zoogdierembryo De verhoging van het minimumloon in Seattle heeft de misdaad- of werkgelegenheidscijfers niet veranderd
De verhoging van het minimumloon in Seattle heeft de misdaad- of werkgelegenheidscijfers niet veranderd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

