
Wetenschap
Kristalstructuren van NaCl en MgO:een gedetailleerde analyse
Structuur van natriumchloride (NaCl) en magnesiumoxide (MgO) als vaste stoffen:
Zowel natriumchloride (NaCl) als magnesiumoxide (MgO) zijn ionische verbindingen met een kristalroosterstructuur . Dit betekent dat de samenstellende ionen in een zeer geordend, zich herhalend patroon zijn gerangschikt.
Natriumchloride (NaCl):
* Kristalstructuur: Gezichtsgecentreerd kubisch (FCC) rooster.
* Ionisch arrangement: Natriumkationen (Na+) en chlorideanionen (Cl-) wisselen elkaar af in een verhouding van 1:1. Stel je een 3D-schaakbordpatroon voor waarbij elk ion wordt omringd door zes ionen met de tegenovergestelde lading.
* Verbinding: Sterke elektrostatische aantrekkingskracht tussen tegengesteld geladen ionen.
* Eigenschappen: Hoge smelt- en kookpunten, hard en bros, oplosbaar in water.
Magnesiumoxide (MgO):
* Kristalstructuur: Vergelijkbaar met NaCl, met een kubisch rooster in het gezicht gecentreerd.
* Ionisch arrangement: Magnesiumkationen (Mg2+) en oxide-anionen (O2-) wisselen elkaar af in een verhouding van 1:1. De opstelling wijkt echter enigszins af van die van NaCl vanwege de verschillende ladingen van de ionen.
* Verbinding: Nog sterkere elektrostatische aantrekkingskracht dan in NaCl vanwege de hogere ladingen van de ionen.
* Eigenschappen: Zeer hoge smelt- en kookpunten, extreem hard en bros, onoplosbaar in water.
Overeenkomsten:
* Beide hebben kubieke kristalstructuren.
* Beide zijn ionische verbindingen met sterke elektrostatische krachten die ze bij elkaar houden.
* Beide hebben hoge smelt- en kookpunten vanwege de sterke ionische bindingen.
Verschillen:
* Grootte van ionen: Mg2+ en O2- zijn kleiner dan Na+ en Cl-, wat leidt tot een dichtere pakking in MgO.
* Lading van ionen: Mg2+ en O2- hebben hogere ladingen dan Na+ en Cl-, wat resulteert in sterkere elektrostatische krachten en een hoger smeltpunt in MgO.
* Oplosbaarheid: NaCl is oplosbaar in water, terwijl MgO onoplosbaar is.
Samenvattend hebben zowel NaCl als MgO vergelijkbare kristalstructuren, maar de verschillen in ionische grootte en lading leiden tot verschillende eigenschappen, vooral in termen van smeltpunt en oplosbaarheid.
 Is zure regen goed of slecht?
Is zure regen goed of slecht?  Hoeveel atomen zitten er in één enkel molecuul Na3P?
Hoeveel atomen zitten er in één enkel molecuul Na3P?  Vormt metaal waarschijnlijk een ion door elektronen te verliezen of te winnen?
Vormt metaal waarschijnlijk een ion door elektronen te verliezen of te winnen?  Wat is de minimale teprature voor kwik?
Wat is de minimale teprature voor kwik?  Wat is een verbinding die veranderingen in de pH minimaliseert door ionen omkeerbaar in te nemen of uit te brengen?
Wat is een verbinding die veranderingen in de pH minimaliseert door ionen omkeerbaar in te nemen of uit te brengen?
Hoofdlijnen
- Wat is het uitscheidingsproduct van Amoeba?
- Waarom endonuclease -enzym dNA tussen 5 en 3 snijden?
- Prokaryotische cellen:cellen zonder kern begrijpen
- Kombucha:Wat het is, waar komt het vandaan
- Kenmerken van een organisme waarmee het effectiever in zijn omgeving kan functioneren?
- Wat is een biochemische basis. Wanneer mensen u vragen naar de basis van het biologische proces, wat betekent dit?
- Verloren of uitgestorven? Uit onderzoek blijkt dat het bestaan van meer dan 500 diersoorten onzeker blijft
- Welke cel vormt osseous weefsel?
- Een phylum wordt altijd geassocieerd?
- Studie toont potentieel voor milieuvriendelijke vervanging van plastic

- Een nieuwe strategie voor de synthese van complexe natuurlijke producten
- Haaibestendig materiaal voor wetsuits kan levens helpen redden

- Kettinglengte bepaalt moleculaire kleur, kleurafstemming voor medische beeldvorming mogelijk maken

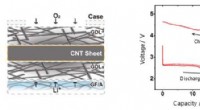
- Ontwikkeling van lithium-luchtbatterijen met ultrahoge capaciteit met behulp van CNT-blad-luchtelektroden
 Natriumchloride (NaCl):de meest voorkomende natriumverbinding - Eigenschappen en toepassingen
Natriumchloride (NaCl):de meest voorkomende natriumverbinding - Eigenschappen en toepassingen  Wat zijn de planeten van de kleinste tot de grootste diameter?
Wat zijn de planeten van de kleinste tot de grootste diameter?  De overdracht van energie in de vorm onzichtbare golven is geleiding waar of onwaar?
De overdracht van energie in de vorm onzichtbare golven is geleiding waar of onwaar?  Zonnepanelen ter grootte van een vlo ingebed in kleding kunnen een mobiele telefoon opladen
Zonnepanelen ter grootte van een vlo ingebed in kleding kunnen een mobiele telefoon opladen Hoe helpen eiwitten ons?
Hoe helpen eiwitten ons?  Hoe meet ik metrische bouten
Hoe meet ik metrische bouten Amazon om 100 in te huren, 000 werknemers om aan de vraag naar het coronavirus te voldoen
Amazon om 100 in te huren, 000 werknemers om aan de vraag naar het coronavirus te voldoen SimRadar:een polarimetrische radar-tijdreekssimulator voor tornadisch puinonderzoek
SimRadar:een polarimetrische radar-tijdreekssimulator voor tornadisch puinonderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

