
Wetenschap
Geconcentreerd zwavelzuur begrijpen:kookpunt en viscositeit
1. Sterke waterstofbinding:
* Structuur: Zwavelzuur heeft twee hydroxylgroepen (-OH) gehecht aan zijn zwavelatoom. Deze hydroxylgroepen zijn zeer polair vanwege het elektronegativiteitsverschil tussen zuurstof en waterstof.
* Waterstofbinding: De sterk gepolariseerde waterstofatomen in de hydroxylgroepen vormen sterke waterstofbruggen met de zuurstofatomen in aangrenzende zwavelzuurmoleculen. Deze waterstofbruggen zijn veel sterker dan de dipool-dipoolinteracties die in veel andere zuren voorkomen.
2. Hoog molecuulgewicht:
* Zwavelzuur heeft een relatief hoog molecuulgewicht vergeleken met veel andere veel voorkomende zuren. Dit draagt bij aan sterkere intermoleculaire krachten.
3. Polariteit:
* Zwavelzuur is zeer polair vanwege het elektronegativiteitsverschil tussen de zwavel- en zuurstofatomen. Deze polariteit versterkt de intermoleculaire aantrekkingskracht verder.
Kookpunt en viscositeit:
* Kookpunt: Voor het overwinnen van een sterke waterstofbinding is een aanzienlijke hoeveelheid energie nodig, wat leidt tot een hoog kookpunt.
* Viscositeit: De sterke intermoleculaire krachten in geconcentreerd zwavelzuur maken het voor moleculen erg moeilijk om langs elkaar heen te glijden. Dit resulteert in een hoge viscositeit, wat betekent dat het langzaam vloeit en bestand is tegen vervorming.
Samengevat:
Het hoge kookpunt en de viscositeit van geconcentreerd zwavelzuur zijn voornamelijk te danken aan de sterke waterstofbinding tussen de moleculen, die verder wordt versterkt door het hoge molecuulgewicht en de hoge polariteit. Dit maakt het een zeer stabiel en bruikbaar zuur in verschillende chemische processen.
 Wat zou er gebeuren met de concentratie van waterstofionen in een oplossing sterk zuur als een gelijk aantal hydroxide werd toegevoegd?
Wat zou er gebeuren met de concentratie van waterstofionen in een oplossing sterk zuur als een gelijk aantal hydroxide werd toegevoegd?  Samengestelde directe objecten begrijpen:definitie en voorbeelden
Samengestelde directe objecten begrijpen:definitie en voorbeelden  Wat is de formule voor zuurstof?
Wat is de formule voor zuurstof?  Video:Waarom je geen verse olijven kunt kopen
Video:Waarom je geen verse olijven kunt kopen Wat is de algemene formule van een aromatisch?
Wat is de algemene formule van een aromatisch?
 Onderzoekers bestuderen hoe serotonine de reukzin van sprinkhanen verandert
Onderzoekers bestuderen hoe serotonine de reukzin van sprinkhanen verandert  Er is maar één manier om bosbranden minder krachtig te maken:verwijder het spul dat brandt
Er is maar één manier om bosbranden minder krachtig te maken:verwijder het spul dat brandt Noem twee factoren die ervoor zorgen dat seizoen en klimaat veranderen?
Noem twee factoren die ervoor zorgen dat seizoen en klimaat veranderen?  Korpsfunctionaris:studie nodig van de overstromingsopties van de Missouri River
Korpsfunctionaris:studie nodig van de overstromingsopties van de Missouri River Hoe werkt een menselijk ecosysteem?
Hoe werkt een menselijk ecosysteem?
Hoofdlijnen
- Wat zijn aardappelzymen?
- Genmutaties begrijpen:definities, oorzaken, typen en voorbeelden uit de echte wereld
- Wat is de functie van nucleolus in een cel?
- Wat zijn de vier basisonderdelen voor een menselijke cel?
- Waar wordt de celdeling gebruikt?
- Welk lichaamsgedeelte is de breadbasket?
- Welke structuur richt de activiteiten van de cellen?
- Hoe creoolse talen evolueren, kan afhangen van hoe mensen ze begonnen te gebruiken
- Wat is de structuur en basen van DNA?
- Hydrogel bootst het menselijk brein na met het vermogen om te onthouden en te vergeten
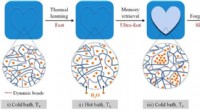
- Wetenschapsprojecten:bevriest suikerwater sneller dan zuiver water?

- COVID-19 testmethode geeft binnen één seconde resultaat

- Een hybride materiaal dat omkeerbaar schakelt tussen twee stabiele vaste toestanden
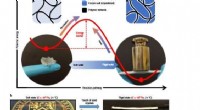
- Methode voor het maken van optisch actieve polymeren met behulp van een spiraalvormig vloeibaar-kristalsjabloon
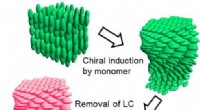
 Wat is de formule voor een molecuul bestaande uit twee waterstofatomen en één zwavelatoom?
Wat is de formule voor een molecuul bestaande uit twee waterstofatomen en één zwavelatoom?  Heeft de zwaartekracht invloed op het meten van het gewicht en de massa van een object op aarde Mars?
Heeft de zwaartekracht invloed op het meten van het gewicht en de massa van een object op aarde Mars?  Wat betekent in de wetenschap?
Wat betekent in de wetenschap?  Wetenschappers gebruiken de Tokyo Skytree om Einsteins algemene relativiteitstheorie te testen
Wetenschappers gebruiken de Tokyo Skytree om Einsteins algemene relativiteitstheorie te testen Welk pH-niveau vertegenwoordigt de hoogste zuurgraad?
Welk pH-niveau vertegenwoordigt de hoogste zuurgraad?  Welke van de volgende moleculen bevat een covalente binding mgO hf hici cn-?
Welke van de volgende moleculen bevat een covalente binding mgO hf hici cn-?  Waarom je baas blank is, uit de middenklasse en een opschepper
Waarom je baas blank is, uit de middenklasse en een opschepper  Op onderzoek gebaseerde strategieën voor het aanleren van vermenigvuldigingsfeiten
Op onderzoek gebaseerde strategieën voor het aanleren van vermenigvuldigingsfeiten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

