
Wetenschap
Conjugaatzuursterkte begrijpen:factoren en voorbeelden
Dit is waarom:
* Sterkere basen hebben zwakkere geconjugeerde zuren. Een sterke base accepteert gemakkelijk protonen (H+), waardoor een relatief stabiel conjugaatzuur achterblijft waarvan het minder waarschijnlijk is dat het een proton teruggeeft.
* Zwakkere basen hebben sterkere geconjugeerde zuren. Het is minder waarschijnlijk dat een zwakke base protonen accepteert, wat resulteert in een geconjugeerd zuur dat eerder een proton zal doneren, waardoor het een sterker zuur wordt.
Voorbeeld:
* Sterke basis: Hydroxide-ion (OH-)
* Zwak conjugaatzuur: Water (H2O)
* Zwakke basis: Ammoniak (NH3)
* Sterk geconjugeerd zuur: Ammoniumion (NH4+)
Om het sterkste geconjugeerde zuur te vinden, moet je het volgende weten:
1. De sterkte van de overeenkomstige basis: Hoe zwakker de base, hoe sterker het geconjugeerde zuur.
2. De specifieke context: Factoren zoals het oplosmiddel en andere reagerende soorten kunnen de zuursterkte beïnvloeden.
Bijvoorbeeld in waterige oplossingen:
* Het sterkste geconjugeerde zuur zou het geconjugeerde zuur van de zwakste base zijn aanwezig. Dit zou zoiets kunnen zijn als H3O+, het geconjugeerde zuur van water.
Laat het me weten als je een specifieke situatie in gedachten hebt, dan kan ik je helpen het sterkste conjugaatzuur te bepalen!
 Welke drie dingen moet je altijd doen bij het hanteren van zuur of alkali in een lab?
Welke drie dingen moet je altijd doen bij het hanteren van zuur of alkali in een lab?  Welke verbindingen elueert eerst in de niet -polaire GC -kolom?
Welke verbindingen elueert eerst in de niet -polaire GC -kolom?  Wat is het verschil tussen goud en stof?
Wat is het verschil tussen goud en stof?  Waarom is het atoom van technetium elektrisch neutraal?
Waarom is het atoom van technetium elektrisch neutraal?  Niet -metalen worden zwak aangetrokken tot elkaar zodat ze welke smelten en kookpunten hebben?
Niet -metalen worden zwak aangetrokken tot elkaar zodat ze welke smelten en kookpunten hebben?
 Duizenden trekken naar IJslands uitbarstende vulkaan
Duizenden trekken naar IJslands uitbarstende vulkaan Bedrijven denken dat ze bovenop het koolstofrisico zitten, maar toeristische bestemmingen hebben nauwelijks een idee
Bedrijven denken dat ze bovenop het koolstofrisico zitten, maar toeristische bestemmingen hebben nauwelijks een idee Koolstofterugkoppeling van bosbodems zal de opwarming van de aarde versnellen, 26-jarige studieprojecten
Koolstofterugkoppeling van bosbodems zal de opwarming van de aarde versnellen, 26-jarige studieprojecten Hoe beïnvloedt natuurlijke fenomenen uw leven?
Hoe beïnvloedt natuurlijke fenomenen uw leven?  Sociaal-economisch onderzoek kijkt naar het vergroten van de betrouwbaarheid van het Panamakanaal
Sociaal-economisch onderzoek kijkt naar het vergroten van de betrouwbaarheid van het Panamakanaal
Hoofdlijnen
- Kun jij de vier belangrijkste biomen van BC noemen?
- Wat doen mariene biologen precies?
- Welke structuur in de cel bevat spijsverteringsenzymen die koolhydraten afbreken?
- Verborgen spelers in de klimaatverandering:hoe microscopische eiwitten onze toekomst kunnen vormgeven
- Staafvormige lichamen die genetische info dragen?
- Welke organismen produceren hun eigen voedsel?
- Welk onderwerp wordt de centrale wetenschap genoemd?
- Wat doet de lichaamsbuis van een microscoop?
- Wat maakt rode algen voor ons?
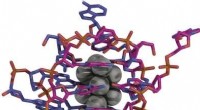
- Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster
- Nieuwe fluorescerende kleurstoffen kunnen biologische beeldvorming bevorderen

- Techniek kan helpen bij massaproductie van biologisch afbreekbaar plastic

- Slim medicijnontwerp om resistentie tegen malariabehandeling te voorkomen

- Kerosinekwaliteiten begrijpen:1-K versus 2-K en hun veiligheidsimplicaties

 Berekening van relatieve frequentieverdeling
Berekening van relatieve frequentieverdeling Aaí bessenextracten bestrijden malaria bij muizen
Aaí bessenextracten bestrijden malaria bij muizen Welke fase van de maan zou het beste en het slechtst zijn om te studeren?
Welke fase van de maan zou het beste en het slechtst zijn om te studeren?  Welk materiaal is erg elastisch?
Welk materiaal is erg elastisch?  Imitatie en versterkend leren gebruiken om robottaken met een lange horizon aan te pakken
Imitatie en versterkend leren gebruiken om robottaken met een lange horizon aan te pakken Versnelling van vrije val als gevolg van zwaartekracht?
Versnelling van vrije val als gevolg van zwaartekracht?  Renault beëindigt Ghosn-tijdperk met winstdaling door Nissan
Renault beëindigt Ghosn-tijdperk met winstdaling door Nissan Hoe ruimteafval op te ruimen – met behulp van speltheorie
Hoe ruimteafval op te ruimen – met behulp van speltheorie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

