
Wetenschap
Metaalbinding en hoge smeltpunten in metalen:een verklaring
* Metaalbinding: Bij metallische bindingen worden de valentie-elektronen van metaalatomen gedelokaliseerd en vormen ze een "zee" van elektronen die vrij zijn om door de gehele metaalstructuur te bewegen. Hierdoor ontstaat er een sterke, niet-gerichte aantrekkingskracht tussen de positief geladen metaalionen en de negatief geladen elektronenzee.
* Hoge smeltpunten: De sterke elektrostatische aantrekkingskracht tussen de ionen en de elektronenzee vereist een aanzienlijke hoeveelheid energie om te overwinnen. Dit betekent dat er veel warmte nodig is om de metaalverbindingen te verbreken en het metaal van vast naar vloeibaar te maken.
Andere soorten verbindingen:
* Ionische binding: Hoewel ionische bindingen sterk zijn, zijn ze over het algemeen zwakker dan metaalbindingen.
* Covalente binding: Covalente bindingen zijn erg sterk binnen het molecuul, maar de krachten tussen moleculen zijn zwakker.
* Van der Waals krachten: Dit zijn zeer zwakke krachten die bijdragen aan de aantrekkingskracht tussen moleculen.
Samenvattend zorgt de sterke en niet-directionele aard van metaalverbindingen ervoor dat metalen hoge smeltpunten hebben.
 Onderzoek naar neutronenverstrooiing wijst de weg naar elektrochemisch voor koolstofneutrale ammoniak
Onderzoek naar neutronenverstrooiing wijst de weg naar elektrochemisch voor koolstofneutrale ammoniak  Wat doen waterstofperoxide en suiker?
Wat doen waterstofperoxide en suiker?  Van welke laag wordt aangenomen dat het zich het meest als een vloeistof gedraagt?
Van welke laag wordt aangenomen dat het zich het meest als een vloeistof gedraagt?  Waar vind je protonen?
Waar vind je protonen?  Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
 Naar huis vliegen? De ijstijd heeft mogelijk de vogelmigratie afgeremd
Naar huis vliegen? De ijstijd heeft mogelijk de vogelmigratie afgeremd  Slushy ijsbergaggregaten regelen de afkalftijd op Groenlands Jakobshavn Isbræ
Slushy ijsbergaggregaten regelen de afkalftijd op Groenlands Jakobshavn Isbræ Ontwikkeling kan de impact van de hittegolf verminderen
Ontwikkeling kan de impact van de hittegolf verminderen Van de grond naar de lucht:onderzoekers kwantificeren de hoeveelheid energie die planten gebruiken om op wereldschaal water op te tillen
Van de grond naar de lucht:onderzoekers kwantificeren de hoeveelheid energie die planten gebruiken om op wereldschaal water op te tillen  7 Classificaties van Earthworms
7 Classificaties van Earthworms
Hoofdlijnen
- Organismen worden geclassificeerd als schimmels als zij?
- Wat zijn Plaisade -cellen?
- Dingo? Bingo! Hoe je dingo vanuit je huis kunt helpen met onderzoek
- Celstructuren en hun drie belangrijkste functies
- Beschrijf het effect van omgevingscondities op de celcyclus?
- Hoe suikervacht die een middel voor cellulaire herkenning biedt, staat bekend als de?
- Leven gelukkige mensen langer?
- Niet-duurzame voedselsystemen:kunnen we de huidige trends omkeren?
- Wie is de gerelateerde persoon van Organelle Nucleus?
- Afstotend onderzoek:marine ontwikkelt scheepscoatings om brandstof te verminderen, energiekosten

- Nieuwe ontwikkelingen in het zoeken naar moleculaire magneten
- Oude eiwitten bieden aanwijzingen voor het verleden

- Nieuwe manier om littekens op de huid te verminderen, is gebaseerd op een lijmachtige substantie die wordt afgescheiden door mosselen

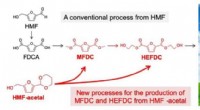
- Groene plastic productie gemakkelijk gemaakt
 Anemometer lezen
Anemometer lezen Stockholm Nobel-ceremonie vervangen door televisie-evenement:Foundation
Stockholm Nobel-ceremonie vervangen door televisie-evenement:Foundation Buigen of buigen lichtgolven op wat tussen twee media?
Buigen of buigen lichtgolven op wat tussen twee media?  Plasticvervuiling in Nigeria:Wiens taak is het om de rommel op te ruimen?
Plasticvervuiling in Nigeria:Wiens taak is het om de rommel op te ruimen?  Wat zijn de primaire bronnen van warmte die geologische processen op aarde aansturen?
Wat zijn de primaire bronnen van warmte die geologische processen op aarde aansturen?  Fossiele brandstoffen veroorzaken een crisis in de kosten van levensonderhoud:klimaatexpert
Fossiele brandstoffen veroorzaken een crisis in de kosten van levensonderhoud:klimaatexpert Hoe vindt u de correlatiecoëfficiënt voor R in een spreidingsdiagram
Hoe vindt u de correlatiecoëfficiënt voor R in een spreidingsdiagram Waarom geeft de ESRT -grafiek kenmerken voor elk mineraal dat op aarde wordt gevonden?
Waarom geeft de ESRT -grafiek kenmerken voor elk mineraal dat op aarde wordt gevonden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

