
Wetenschap
Normaliteit berekenen:Na₂CO₃-massa bepalen voor een oplossing van 0,02 N
Normaliteit begrijpen (N)
* Normaliteit is een concentratie-eenheid die het aantal equivalenten van een opgeloste stof per liter oplossing meet.
* Een equivalent is de hoeveelheid van een stof die kan reageren met één mol waterstofionen (H⁺) of hydroxide-ionen (OH⁻) of deze kan vervangen.
Na₂CO₃ en equivalenten
* Natriumcarbonaat (Na₂CO₃) is een base. Wanneer het oplost in water, reageert het met water en produceert het carbonaationen (CO₃²⁻), die twee waterstofionen (H⁺) kunnen opnemen.
* Daarom is één mol Na₂CO₃ gelijk aan twee equivalenten (omdat het twee mol H⁺ kan accepteren).
De benodigde massa berekenen
1. Molar massa van Na₂CO₃: 105,99 g/mol
2. Equivalenten per mol: 2 equivalenten/mol (zoals hierboven uitgelegd)
3. Gewenste normaliteit: 0,02 N
4. Volume van de oplossing: 1 liter
Berekeningen:
* Gram Na₂CO₃ nodig: (0,02 N) * (1 L) * (105,99 g/mol) / (2 equivalenten/mol) =1,06 g
Conclusie
Door 1,06 g Na₂CO₃ toe te voegen aan 1 liter water ontstaat een oplossing van 0,02 N, omdat deze massa het juiste aantal equivalenten Na₂CO₃ levert om de gewenste normaliteit te bereiken.
 Onderzoek onderzoekt hoe betekenisvolle maar ongebruikte producten duurzaamheid belemmeren
Onderzoek onderzoekt hoe betekenisvolle maar ongebruikte producten duurzaamheid belemmeren  Recente klimaatextremen hebben geleid tot ongekende veranderingen in de diepe oceaan
Recente klimaatextremen hebben geleid tot ongekende veranderingen in de diepe oceaan Academische oproepen tot upgrade van rioleringssystemen om de gezondheid te beschermen
Academische oproepen tot upgrade van rioleringssystemen om de gezondheid te beschermen  De effecten van tyfoons
De effecten van tyfoons  Het tijdperk van fossiele brandstoffen loopt ten einde, maar de rechtszaken zijn nog maar net begonnen
Het tijdperk van fossiele brandstoffen loopt ten einde, maar de rechtszaken zijn nog maar net begonnen
Hoofdlijnen
- Wilde genen bij gedomesticeerde soorten:hoe we onze gewassen een boost kunnen geven met behulp van hun verre verwanten
- Welk stadium van de celcycluscellen verdeelt de kern?
- Hoe reproduceren pinda's zich?
- Zijn de meeste cellen in het menselijk lichaam haploïde of diploïd?
- Welke sequentie in mRNA complementeert de DNA-template?
- Hoe verbeter je in de biologie?
- Een groep organismen die nakomelingen produceren zoals zijzelf?
- Wat zijn de organisatieniveaus die verder gaan dan het niveau van het organisme?
- Waarom classificeren wetenschapper het virus als levende wezens?
- Elektronenmicroscopie onthult de reden voor de paarse vlekken op Alhambra-plafonds

- Onderzoekers krijgen inzicht in hoe enzymen specifieke reacties bereiken
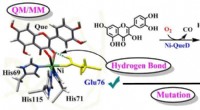
- Verkenning van sojasausen zoutversterkende peptiden

- Upcycling van sponsachtig plastic schuim van schoenen, matrassen en isolatie

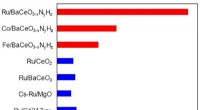
- Efficiënte bottom-up synthese van nieuw perovskietmateriaal voor de productie van ammoniak
 Waarom zijn elliptische sterrenstelsels zo groot?
Waarom zijn elliptische sterrenstelsels zo groot?  Gevoeligere modellering voor betere economische prognoses
Gevoeligere modellering voor betere economische prognoses Ongelijke mate van zeespiegelstijging gekoppeld aan klimaatverandering
Ongelijke mate van zeespiegelstijging gekoppeld aan klimaatverandering Wat is een functie gemaakt door glaciale afwijzingen?
Wat is een functie gemaakt door glaciale afwijzingen?  Temporal-spatial order-eigenschap van holle multishelled-structuren maakt sequentiële medicijnafgifte mogelijk
Temporal-spatial order-eigenschap van holle multishelled-structuren maakt sequentiële medicijnafgifte mogelijk Wat is onder de troposfeer?
Wat is onder de troposfeer?  Kan de maan op elk moment overal worden gezien?
Kan de maan op elk moment overal worden gezien?  Wat is een goed gemengd mengsel dat een enkele stof lijkt te zijn?
Wat is een goed gemengd mengsel dat een enkele stof lijkt te zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

