
Wetenschap
Molariteit versus normaliteit:wat is meer geconcentreerd voor H2SO4?
Molariteit en normaliteit begrijpen
* Molariteit (M): Vertegenwoordigt het aantal mol opgeloste stof per liter oplossing.
* Normaliteit (N): Vertegenwoordigt het aantal equivalenten opgeloste stof per liter oplossing.
Belangrijkste verschil: Normaliteit houdt rekening met het aantal *reactieve eenheden* (bijvoorbeeld H+-ionen) dat een molecuul bijdraagt aan een reactie.
Voorbeeld H2SO4 (zwavelzuur)
* Molariteit: Een 1 M H2SO4-oplossing bevat 1 mol H2SO4 per liter oplossing.
* Normaliteit: Een 1 N H2SO4-oplossing bevat 2 equivalenten H+-ionen per liter oplossing (aangezien H2SO4 2 zure waterstofatomen heeft).
Conclusie
Omdat een 1 N H2SO4-oplossing 2 equivalenten H+-ionen per liter bevat, terwijl een 1 M H2SO4-oplossing 1 mol H2SO4 per liter bevat, is de 1 N H2SO4-oplossing meer geconcentreerd in termen van reactieve eenheden (H+-ionen).
 CeCoIn5 onthult nieuwe geheimen over hoe supergeleiding en magnetisme met elkaar in verband kunnen worden gebracht
CeCoIn5 onthult nieuwe geheimen over hoe supergeleiding en magnetisme met elkaar in verband kunnen worden gebracht  Belangrijke instrumenten die meteorologen gebruiken om het weer te voorspellen
Belangrijke instrumenten die meteorologen gebruiken om het weer te voorspellen  Wat is een eigenschap die kan worden gebruikt om metalen van niet-metaalhoudende mineralen te onderscheiden?
Wat is een eigenschap die kan worden gebruikt om metalen van niet-metaalhoudende mineralen te onderscheiden?  Welk type moleculen polair of niet oplost in water?
Welk type moleculen polair of niet oplost in water?  Hoe wordt een molecuul gevormd?
Hoe wordt een molecuul gevormd?
 Waarom gloeien sommige boomwortels in het donker als ze worden blootgesteld?
Waarom gloeien sommige boomwortels in het donker als ze worden blootgesteld?  Opwarming van de aarde veroorzaakt ongelijkmatige veranderingen in indicatoren voor hittestress
Opwarming van de aarde veroorzaakt ongelijkmatige veranderingen in indicatoren voor hittestress Staalsnippers zijn veelbelovend bij het verwijderen van E. coli uit regenwater
Staalsnippers zijn veelbelovend bij het verwijderen van E. coli uit regenwater Orkaan Sally veroorzaakt overstromingen langs de Gulf Coast
Orkaan Sally veroorzaakt overstromingen langs de Gulf Coast Animal Behaviour Science Fair Projectideeën
Animal Behaviour Science Fair Projectideeën
Hoofdlijnen
- Eerste bevestigde waarneming van boommarter op Anglesey in meer dan 30 jaar
- Waarom kunnen dierencellen hun eigen organische voedsel niet maken?
- Ohio's verdwijnende dieren in het wild:soorten die zijn uitgestorven en de lessen die ze bieden
- Hoe warmere wateren als gevolg van klimaatverandering de biochemie en de groei van vissen beïnvloeden
- Spanje meldt geval van gekkekoeienziekte
- Waar bestaat elk nucleotide in een DNA -streng uit?
- Wat zijn twee voorbeelden van gespecialiseerde cellen en verklaren de unieke rol in het menselijk lichaam?
- Nieuwe technologie maakt detectie van eikenverwelking sneller, betaalbaarder
- Hoe bacteriën hypothiocyaniet onschadelijk maken, een antimicrobieel wapen van het aangeboren immuunsysteem
- Water vervangt gifstoffen:groene productie van plastic

- Het nieuwe peptide van biologen kan veel kankers bestrijden
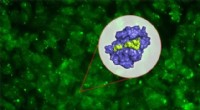
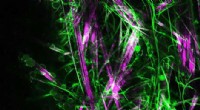
- Een nieuw gelerend molecuul voor het kweken van neuronen in 3-D
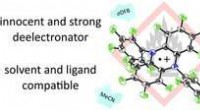
- Chemici produceren nieuwe oxidanten als hulpmiddel voor preparatieve chemie
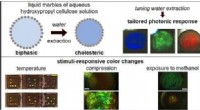
- Cellulose:een altijd aanwezig materiaal met opmerkelijke eigenschappen
 Spuitbare gel kan het lichaam helpen kanker na een operatie te bestrijden
Spuitbare gel kan het lichaam helpen kanker na een operatie te bestrijden Welke toestand van materie wordt gekenmerkt door een duidelijke vorm en volume te hebben?
Welke toestand van materie wordt gekenmerkt door een duidelijke vorm en volume te hebben?  Wat is het doel van biotechnologie?
Wat is het doel van biotechnologie?  Satellietvolging laat zien hoe schepen de wolken en het klimaat beïnvloeden
Satellietvolging laat zien hoe schepen de wolken en het klimaat beïnvloeden Plastic in rivieren belangrijkste bron van oceaanvervuiling:studie
Plastic in rivieren belangrijkste bron van oceaanvervuiling:studie Wat is constructieve erosie?
Wat is constructieve erosie?  Wat voor soort insecten leven in het bladverliezende bos?
Wat voor soort insecten leven in het bladverliezende bos?  Variëren de verschillende vormen van elektromagnetische energie in hun 1 golflengten 2 snelheid 3 deeltjesgrootte 4 vermogen om door de ruimte te gaan?
Variëren de verschillende vormen van elektromagnetische energie in hun 1 golflengten 2 snelheid 3 deeltjesgrootte 4 vermogen om door de ruimte te gaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

