
Wetenschap
Acetyleen- en lachgasreactie:vergelijking, producten en uitleg
Hier is een vereenvoudigde weergave van de reactie, die zich richt op de primaire producten:
C₂H₂ + 2 N₂O → 2 CO₂ + H₂O + 2 N₂
Uitleg:
* Acetyleen (C₂H₂): De brandstofbron.
* Lachgas (N₂O): De oxidator, die de zuurstof levert voor verbranding.
* Kooldioxide (CO₂): Het primaire product van de verbranding van de koolstofatomen in acetyleen.
* Water (H₂O): Het primaire product van de verbranding van de waterstofatomen in acetyleen.
* Stikstof (N₂): Het product van de ontleding van lachgas.
Belangrijke overwegingen:
* Verbrandingstemperatuur: De reactie vereist een hoge temperatuur om te starten. Dit wordt doorgaans bereikt door gebruik te maken van een vonk of vlam.
* Reactiemechanisme: Het eigenlijke mechanisme is complexer en omvat meerdere tussenstappen, die mogelijk kunnen leiden tot de vorming van andere producten zoals stikstofoxiden (NOx).
* Stoichiometrie: De exacte verhouding van de reactanten die nodig zijn voor volledige verbranding kan enigszins variëren, afhankelijk van de reactieomstandigheden.
Toepassingen:
Deze reactie wordt vaak gebruikt bij:
* Gaslassen: Acetyleen en lachgas worden gebruikt als brandstof-oxidatiemiddelcombinatie bij lasprocessen.
* Gassnijden: De hoge temperatuur die door deze reactie wordt gegenereerd, kan worden gebruikt voor het snijden van metalen.
Houd er rekening mee dat dit een vereenvoudigde weergave is en dat de feitelijke reactie ingewikkelder is. Voor specifieke toepassingen en gedetailleerde analyses is het belangrijk om experts of uitgebreide literatuur over chemische technologie te raadplegen.
 Koper bij kamertemperatuur:vaste toestand uitgelegd
Koper bij kamertemperatuur:vaste toestand uitgelegd  Waarom brengen we chemische vergelijkingen in evenwicht?
Waarom brengen we chemische vergelijkingen in evenwicht?  Waarom kan water niet worden gebruikt om natriumthiosulfaatoplossing te bereiden?
Waarom kan water niet worden gebruikt om natriumthiosulfaatoplossing te bereiden?  Germanium:eigenschappen, gebruik en belang in technologie
Germanium:eigenschappen, gebruik en belang in technologie  Onderzoekers vinden nieuwe manier om griepvirus aan te pakken
Onderzoekers vinden nieuwe manier om griepvirus aan te pakken
 meer vee, meer kooldioxide, minder ijs:de vooruitgang van de klimaatverandering in de wereld sinds 2019
meer vee, meer kooldioxide, minder ijs:de vooruitgang van de klimaatverandering in de wereld sinds 2019 NASA vindt windschering in tropische storm Gabekile
NASA vindt windschering in tropische storm Gabekile COVID-19-lockdowns gekoppeld aan vervuilingspieken in sommige steden
COVID-19-lockdowns gekoppeld aan vervuilingspieken in sommige steden Zingen in de regen:waarom bundengan nat beter klinkt
Zingen in de regen:waarom bundengan nat beter klinkt  Alle dingen zullen ons overleven:hoe het inheemse concept van diepe tijd ons helpt de vernietiging van het milieu te begrijpen
Alle dingen zullen ons overleven:hoe het inheemse concept van diepe tijd ons helpt de vernietiging van het milieu te begrijpen
Hoofdlijnen
- Cellulaire ademhaling:de tegenhanger van fotosynthese uitgelegd
- Welke rol speelde de microscoop I ontwikkeling van de celtheorie?
- Spierweefsel bestaat uit cellen die zeer gespecialiseerd zijn voor de functie van?
- Informatie over het maken van eiwitten bevindt zich in het Golgi -complex of kern?
- Wat zijn eiwitten die de timing van de celcyclus reguleren in eukaryotische cellen die worden genoemd?
- Wat is een voorbeeld van een goede bacterie?
- Wat is het proces waarin uw lichaam zichzelf reguleert?
- Welk deel van een cel zou je bestuderen als je chromosomen wilde observeren?
- Wordt een plantencel beschouwd als veel cellen organisme?
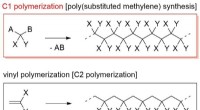
- Ontwikkeling van nieuwe slimme zachte materialen:Synthese van een pH-responsief gedendroniseerd poly(gesubstitueerd methyleen)s
- Van kegelslakkengif tot pijnverlichting

- Drugsgebruiktrends vroeg in de COVID-19-pandemie wegspoelen

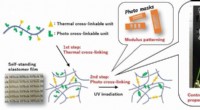
- Films ontwikkelen met instelbare rek en breuk voor verschillende toepassingen
- Hoe goud biobrandstofafval kan recyclen tot nuttig additief

 Is het veranderen van een cent goud een chemische of fysische reactie?
Is het veranderen van een cent goud een chemische of fysische reactie?  Wat is de definitie van organisme?
Wat is de definitie van organisme?  Welk metaal wordt verkregen in het ertsmagnetiet?
Welk metaal wordt verkregen in het ertsmagnetiet?  Welk type energie veroorzaakt te trillen?
Welk type energie veroorzaakt te trillen?  Werd eerst een vliegtuig of een raket uitgevonden?
Werd eerst een vliegtuig of een raket uitgevonden?  Waar zijn enkele manieren waarop thermische energie wordt gebruikt?
Waar zijn enkele manieren waarop thermische energie wordt gebruikt?  Wat zijn de 3 voorbeelden van stam-tendril-planten?
Wat zijn de 3 voorbeelden van stam-tendril-planten?  Waarom is kleur belangrijk van aard?
Waarom is kleur belangrijk van aard?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

