
Wetenschap
Elektronenverlies in hoofdgroepmetalen:s-orbitalen versus d-orbitalen
* Elektronenconfiguratie: Metalen uit de hoofdgroep hebben hun valentie-elektronen in de s- en p-orbitalen. De d-subshell is gevuld vóór de s- en p-orbitalen in de overgangsmetalen van periode 4, maar maakt geen deel uit van de valentie-elektronenconfiguratie voor metalen uit de hoofdgroep.
* Ionisatie-energie: De ionisatie-energie (de energie die nodig is om een elektron te verwijderen) is over het algemeen lager voor s-elektronen dan voor d-elektronen. Dit komt omdat s-elektronen verder van de kern verwijderd zijn en een minder effectieve nucleaire lading ervaren (de aantrekkingskracht tussen de kern en elektronen).
* Stabiliteit: Het verliezen van elektronen uit de s-subshell leidt tot een stabielere elektronenconfiguratie voor metalen uit de hoofdgroep, omdat ze streven naar een edelgasconfiguratie.
Voorbeeld: Tin (Sn) heeft de elektronenconfiguratie [Kr] 4d¹⁰ 5s² 5p². Wanneer het een kation vormt, verliest het eerst de twee 5p-elektronen, gevolgd door de twee 5s-elektronen.
Belangrijke opmerking: Hoewel metalen uit de hoofdgroep niet eerst d-elektronen verliezen, kunnen er wel d-orbitalen bij de binding betrokken zijn. Sn kan bijvoorbeeld Sn²⁺- of Sn⁴⁺-ionen vormen, maar kan ook deelnemen aan covalente bindingen met behulp van zijn d-orbitalen.
Samenvattend is de neiging van metalen uit de hoofdgroep om eerst elektronen uit hun s- en p-subschillen te verliezen, en niet uit de d-subschil.
Hoofdlijnen
- Inprokaryoten:hoe verschillen binaire splitsing en conjugatie?
- Welke van postulaten over evolutie door natuurlijke selectie is het meest direct gerelateerd aan differentiaal reproductief succes?
- Waarom zijn de mentale afbeeldingen die wetenschappers nuttig gebruiken?
- Nieuw mechanisme verduidelijkt hoe cellen migreren
- Mariene microbiële populaties:potentiële sensoren van de mondiale verandering in de oceaan
- Wat voor soort ziekte is tyfus?
- Hoe vissen evolueerden om te lopen
- Kan discriminatie bijdragen aan gevoelens van radicalisering?
- Hoe vergif Sumac te behandelen?
- Eigenschappen van CO2-clathraathydraat
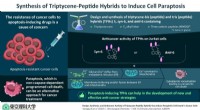
- Geprogrammeerde celdood in kankercellen:weerstand overwinnen door paraptose-inducerende verbindingen
- De fundamentele mechanismen van menselijke speekselsmering decoderen
- Video:Waarom haten sommige mensen koriander?

- Wetenschappers ontwikkelen biologisch actieve verbindingen voor een antitumormiddel
 Waarom zijn objecten die in de buurt van de aarde vallen en zelden in vrije zwaartekracht niet op het oppervlak werken. Lucht oefent krachten uit die zijn?
Waarom zijn objecten die in de buurt van de aarde vallen en zelden in vrije zwaartekracht niet op het oppervlak werken. Lucht oefent krachten uit die zijn?  Waarom spiegelt de complexiteit van genregulatie organisme waarin het wordt gevonden?
Waarom spiegelt de complexiteit van genregulatie organisme waarin het wordt gevonden?  Exotische koolstofmicrokristallen in meteorietstof
Exotische koolstofmicrokristallen in meteorietstof Exomoons zijn mogelijk de thuisbasis van buitenaards leven
Exomoons zijn mogelijk de thuisbasis van buitenaards leven Siliciumalternatieven sleutel tot toekomstige computers, consumentenelektronica
Siliciumalternatieven sleutel tot toekomstige computers, consumentenelektronica Welke van de volgende helderheidsklassen verwijst naar sterren op de hoofdreeks?
Welke van de volgende helderheidsklassen verwijst naar sterren op de hoofdreeks?  Accenture lanceert nieuwe tool om klanten te helpen oneerlijke vooroordelen in AI-algoritmen te identificeren en op te lossen
Accenture lanceert nieuwe tool om klanten te helpen oneerlijke vooroordelen in AI-algoritmen te identificeren en op te lossen Wat wordt bedoeld met vibrerende beweging?
Wat wordt bedoeld met vibrerende beweging?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


