
Wetenschap
Ionische geleidbaarheid in oplossingen:het mechanisme begrijpen
1. Oplossen: Wanneer een ionische verbinding zoals natriumchloride (NaCl) oplost in water, wordt de sterke elektrostatische aantrekkingskracht tussen de positieve natriumionen (Na+) en negatieve chloride-ionen (Cl-) overwonnen door de polaire watermoleculen.
2. Dissociatie: De watermoleculen omringen en scheiden de ionen, waardoor de ionische binding effectief wordt verbroken en individuele, mobiele ionen in oplossing worden gevormd.
3. Geleidbaarheid: Deze vrije ionen kunnen onafhankelijk bewegen binnen de oplossing. Wanneer een elektrische potentiaal over de oplossing wordt aangelegd, bewegen de positieve ionen naar de negatieve elektrode (kathode) en de negatieve ionen naar de positieve elektrode (anode). Deze stroom geladen deeltjes vormt een elektrische stroom.
Belangrijkste punten:
* Vrije ionen zijn essentieel: Het vermogen van ionische verbindingen om elektriciteit in oplossing te geleiden, is afhankelijk van de aanwezigheid van vrije, mobiele ionen.
* Vaste ionische verbindingen geleiden niet: In hun vaste toestand zijn de ionen gefixeerd in een kristallijn rooster en kunnen ze niet vrij bewegen.
* Elektrolyten: Oplossingen die ionische verbindingen bevatten die elektriciteit geleiden, worden elektrolyten genoemd.
Samenvattend is het vermogen van ionische verbindingen om elektriciteit in oplossing te geleiden te danken aan de vorming van vrije, mobiele ionen wanneer ze dissociëren. Deze ionen kunnen vervolgens onder invloed van een elektrisch veld een elektrische stroom transporteren.
 Wat zijn de fasen van de maan?
Wat zijn de fasen van de maan?  Traditionele vaardigheden helpen mensen op de verstokte eilanden in de Stille Oceaan om de pandemie te overleven
Traditionele vaardigheden helpen mensen op de verstokte eilanden in de Stille Oceaan om de pandemie te overleven GPM-satelliet ziet tropische cycloon Son-Tinh regen laten vallen in de Filippijnen
GPM-satelliet ziet tropische cycloon Son-Tinh regen laten vallen in de Filippijnen Overconsumptie en groei economie belangrijkste aanjagers van milieucrises
Overconsumptie en groei economie belangrijkste aanjagers van milieucrises Zeegras bespaart stranden en geld
Zeegras bespaart stranden en geld
Hoofdlijnen
- Welke term beschrijft de relatie tussen bijen en bloeiende planten?
- Hoe reageren cellen op micro- en nanoplastics?
- Waarom zijn mutaties in lichaamscellen geen bron van genetische variatie?
- Belangrijke verbeteringen onthuld op Closer to Van Eyck webapplicatie
- Zijn centriolen in zowel planten- als diercellen?
- Wat zit er in je tarwe? Wetenschappers voegen het genoom van de meest voorkomende broodtarwe samen
- Het andere pad van de keel leidt tot longen dat het wordt genoemd?
- Welke rollen spelen eiwitten in levende dingen?
- Is een schimmels groter dan protist?
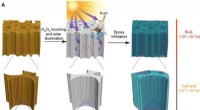
- Een nieuwe manier om hout transparant te maken, sterker en lichter dan glas
- Wat maakt een gigantische kwal dodelijk?

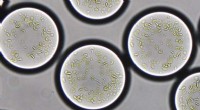
- Onderzoekers ontwikkelen een kunstmatige chloroplast
- Biosensor maakt realtime zuurstofmonitoring mogelijk voor organen-op-een-chip

- Berekening van het terugwinningspercentage van een chemisch product na zuivering

 Gaat suiker in vaste vorm elektriciteit?
Gaat suiker in vaste vorm elektriciteit?  Hoe verbeter je in de biologie?
Hoe verbeter je in de biologie?  Welk deel van de spraak is geologie?
Welk deel van de spraak is geologie?  Studie vindt dat prehistorische mensen beenmerg aten zoals soep uit blik 400, 000 jaar geleden
Studie vindt dat prehistorische mensen beenmerg aten zoals soep uit blik 400, 000 jaar geleden Woede is een rage op Twitter als het buiten koud is (en op maandag)
Woede is een rage op Twitter als het buiten koud is (en op maandag) Nieuwe materialen verbeteren de levering van therapeutisch boodschapper-RNA
Nieuwe materialen verbeteren de levering van therapeutisch boodschapper-RNA Martin Model 130 China Clipper
Martin Model 130 China Clipper  Aantekeningen maken op uw TI‑84 Silver Edition-rekenmachine:een stapsgewijze handleiding
Aantekeningen maken op uw TI‑84 Silver Edition-rekenmachine:een stapsgewijze handleiding
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

