
Wetenschap
Olie en water:begrijpen waarom ze niet samengaan - een wetenschappelijke verklaring
* Polariteit: Watermoleculen zijn polair , wat betekent dat ze een enigszins positief uiteinde en een enigszins negatief uiteinde hebben vanwege de ongelijke verdeling van elektronen. Hierdoor ontstaat er een sterke aantrekkingskracht tussen watermoleculen, waardoor waterstofbruggen ontstaan.
* Niet-polariteit: Oliemoleculen daarentegen zijn niet-polair . Hun elektronen worden gelijkmatiger verdeeld, wat resulteert in geen significante positieve of negatieve ladingen.
Waarom dit belangrijk is:
* Like lost op als: Polaire stoffen hebben de neiging andere polaire stoffen op te lossen, terwijl niet-polaire stoffen andere niet-polaire stoffen oplossen.
* Onmengbaarheid: Omdat water polair is, heeft het geen sterke aantrekkingskracht op de niet-polaire oliemoleculen. In plaats van op te lossen scheiden de twee stoffen zich, waarbij de olie bovenop drijft omdat deze minder dicht is.
Zie het zo: Stel je voor dat je probeert magneten te combineren met niet-magnetische voorwerpen. De magneten zouden aan elkaar blijven plakken en afzonderlijke klonten vormen, terwijl de niet-magnetische objecten gescheiden zouden blijven.
Hetzelfde principe geldt voor olie en water. De sterke aantrekkingskracht tussen watermoleculen verhindert dat ze zich vermengen met olie, waardoor er twee verschillende lagen ontstaan.
 Beschrijf de algemene locatie van elektronen in een covalente binding?
Beschrijf de algemene locatie van elektronen in een covalente binding?  Een soultion van gassen die de aarde bedekt?
Een soultion van gassen die de aarde bedekt?  Onderzoekers vinden verrassende bindingen van het overgangsmetaaltype tijdens het bouwen van nieuwe calcium(I)-complexen
Onderzoekers vinden verrassende bindingen van het overgangsmetaaltype tijdens het bouwen van nieuwe calcium(I)-complexen MOF houdt de vochtigheid in de Goudlokje-zone
MOF houdt de vochtigheid in de Goudlokje-zone Waarom bevriest een NaCl -oplossing bij lagere temperatuur dan water maar kookt hoger water?
Waarom bevriest een NaCl -oplossing bij lagere temperatuur dan water maar kookt hoger water?
 Wat kunnen we specifiek doen om het noordpoolgebied te koelen?
Wat kunnen we specifiek doen om het noordpoolgebied te koelen? Verwoest Venetië zet zich schrap voor derde grote overstroming
Verwoest Venetië zet zich schrap voor derde grote overstroming Microplastics in het wegverkeer overspoelen de oceanen van de wereld:studie
Microplastics in het wegverkeer overspoelen de oceanen van de wereld:studie Verkenning Indische Oceaan maakt historische onderzeese uitzending
Verkenning Indische Oceaan maakt historische onderzeese uitzending Onderzoekers maken met grotere nauwkeurigheid broeikasgasemissies uit tropische veengronden
Onderzoekers maken met grotere nauwkeurigheid broeikasgasemissies uit tropische veengronden
Hoofdlijnen
- Welke 3 elementen worden gevonden in alle biologische macromoleculen?
- Waar staat voor in de biologie?
- Hoe de nucleus controleert de cellulaire functie?
- Beïnvloeden biotisch en abiotisch elkaar?
- Hoe eet Rhizopus?
- Welke giftige stoffen die van nature worden geproduceerd door bacterieplanten slangen insecten en andere levende organismen?
- Is eutrofiëring altijd het gevolg van menselijke activiteit?
- Neanderthaler DNA veranderde de manier waarop moderne mensen eruitzien
- Wat is een celwand op plantencel?
- De oorsprong van chocolade:van het oude Zuid-Amerika tot de moderne productie

- Snelle methode helpt bij het detecteren van Arf6-guanine-nucleotide-uitwisselingsfactoractiviteit
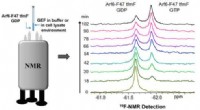
- Wetenschappers ontwikkelen een chemokatalytische benadering voor een-potreactie van cellulose-ethanol
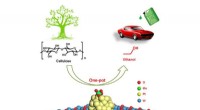
- Ultrastabiel, selectieve katalysator voor propaandehydrogenering ontwikkeld
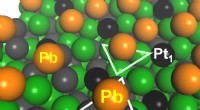
- Synthese van waardevolle chemicaliën uit verontreinigde grond

 Hoe wordt Shale Rock gevormd?
Hoe wordt Shale Rock gevormd?  Wat is een andere naam voor ondergrondse waterbassins?
Wat is een andere naam voor ondergrondse waterbassins?  Wat zijn ecosystemen?
Wat zijn ecosystemen?  Wat voor soort cellen missen een kern?
Wat voor soort cellen missen een kern?  winterslaap voorbij, New Horizons zet Kuiper Belt-cruise voort
winterslaap voorbij, New Horizons zet Kuiper Belt-cruise voort NASA vindt windschering die orkaan Kenneth . verzwakt
NASA vindt windschering die orkaan Kenneth . verzwakt Amerikaanse productie zakt in recessie te midden van handelsoorlogen
Amerikaanse productie zakt in recessie te midden van handelsoorlogen Wat is de periode van een geluidsgolf waarvan de lengte 20,0 m?
Wat is de periode van een geluidsgolf waarvan de lengte 20,0 m?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

