
Wetenschap
Gibbs vrije energievergelijking gebruiken Wat is de verandering voor de synthese van koolstofdisulfide bij 25C?
1. Schrijf de gebalanceerde chemische vergelijking:
De synthese van koolstofdisulfide uit zijn elementen is:
C (s) + 2S (s) → CS₂ (l)
2. Verzamel standaard Gibbs -vrije energie van formatiewaarden:
U hebt de standaard Gibbs -vrije energie -energie -energie nodig (ΔG ° F) voor elke component in de reactie. Deze waarden worden meestal aangetroffen in thermodynamische tabellen. Hier is een gemeenschappelijke reeks waarden:
* ΔG ° F [C (s)] =0 kJ/mol (per definitie is de standaardstatus van een element 0)
* ΔG ° F [s (s)] =0 kJ/mol (hetzelfde als hierboven)
* ΔG ° F [cs₂ (l)] =+65,3 kJ/mol
3. Pas de Gibbs Free Energy -vergelijking toe:
De Gibbs vrije energieverandering voor een reactie (ΔG °) wordt berekend als:
ΔG ° =σNAG ° F (producten) - σmΔG ° F (reactanten)
waar:
* N en M zijn de stoichiometrische coëfficiënten in de evenwichtige vergelijking
* ΔG ° F is de standaard Gibbs -vrije energie van formatie
4. Vervang waarden en bereken:
ΔG ° =(1 * ΔG ° F [cs₂ (l)]) - (1 * ΔG ° F [c (s)] + 2 * ΔG ° F [s (s)])
ΔG ° =(1 * 65,3 kJ/mol) - (1 * 0 kJ/mol + 2 * 0 kJ/mol)
ΔG ° =65,3 kJ/mol
Daarom is de verandering in Gibbs -vrije energie voor de synthese van koolstofdisulfide bij 25 ° C +65,3 kJ/mol.
Interpretatie:
* positief ΔG °: Dit geeft aan dat de reactie niet-spontaan is onder standaardomstandigheden (25 ° C en 1 atm). Met andere woorden, energie -input is vereist om de reactie naar voren te brengen.
belangrijke opmerkingen:
* De Gibbs Free Energy -vergelijking veronderstelt standaardomstandigheden (25 ° C en 1 atm). Voor andere omstandigheden zou u de Gibbs -vrije energievergelijking moeten gebruiken met de juiste temperatuur- en drukwaarden.
* De werkelijke spontaniteit van een reactie kan worden beïnvloed door factoren zoals concentratie, druk en temperatuur. De Gibbs Free Energy -vergelijking biedt een goed startpunt, maar heeft mogelijk aanpassingen nodig voor specifieke omstandigheden.
 Waar komt water dat op de grond is?
Waar komt water dat op de grond is?  Draagtijd voor vogels
Draagtijd voor vogels  5 groene manieren om goederen te vervoeren
5 groene manieren om goederen te vervoeren  Indoor HEPA-filters verminderen de vervuiling binnenshuis aanzienlijk wanneer de buitenlucht ongezond is, studie vondsten
Indoor HEPA-filters verminderen de vervuiling binnenshuis aanzienlijk wanneer de buitenlucht ongezond is, studie vondsten Minder werken om de planeet te redden? Hoe zorg je ervoor dat een vierdaagse werkweek daadwerkelijk de uitstoot vermindert?
Minder werken om de planeet te redden? Hoe zorg je ervoor dat een vierdaagse werkweek daadwerkelijk de uitstoot vermindert?
Hoofdlijnen
- Wat is een lijst van de vierfasenmitose op volgorde?
- Hoe recyclen cellen de machinerie die hun beweeglijkheid aandrijft?
- Wat is het Invetory System?
- Hoe zijn wortels verschillende rhizoïden?
- Wat is nucleair dimorfisme?
- Wat kan je spit je vertellen over je DNA?
- Nieuw boek:Hoe u kunt voorkomen dat STEM-ondersteuning tekortschiet
- Waarom insecten zich kunnen ontwikkelen uit onbevruchte eicellen
- Hoe reproduceren planten zich als ze zaadloos zijn?
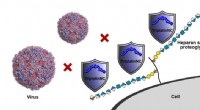
- Op metaal gebaseerde verbindingen maken de weg vrij voor nieuwe antivirale behandelingen
- Metaalzepen kritisch in snelheid van bederf van olieverfschilderijen

- Een onderzoek naar de instabiliteit van het rozenvenster

- Onderzoekers gebruiken nieuwe tools van datawetenschap om afzonderlijke moleculen in actie vast te leggen

- De zon gebruiken om menstruatiearmoede aan te pakken

 Heeft de politie een universiteit nodig?
Heeft de politie een universiteit nodig?  Is er een reactie tussen lithiumjodide en chloor?
Is er een reactie tussen lithiumjodide en chloor?  Genderkloven in de financiering van onderzoek zijn te wijten aan een minder gunstige beoordeling van vrouwen, niet hun wetenschap
Genderkloven in de financiering van onderzoek zijn te wijten aan een minder gunstige beoordeling van vrouwen, niet hun wetenschap Vernietiging van een waargenomen kwantummonopool
Vernietiging van een waargenomen kwantummonopool Hoeveel elektronen in een natriumion?
Hoeveel elektronen in een natriumion?  In hoeveel vormen ontlast?
In hoeveel vormen ontlast?  Ik heb het gedaan:Portugese hacker zegt dat hij Afrikaanse tycoon heeft ontmaskerd
Ik heb het gedaan:Portugese hacker zegt dat hij Afrikaanse tycoon heeft ontmaskerd Is kopersulfaat alkalisch of zuur?
Is kopersulfaat alkalisch of zuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

